Нитрит калия
Нитрит калия
| Нитрит калия | |
|---|---|
 |
|
| Систематическое наименование |
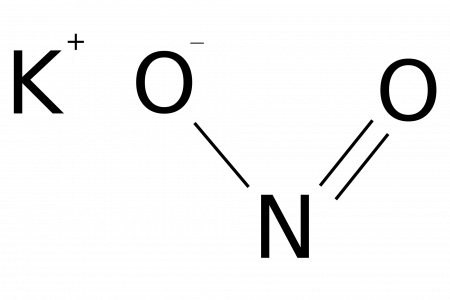
Нитрит калия |
| Традиционные названия | Азотистокислый калий |
| Хим. формула | KNO2 |
| Состояние | прозрачные (белые) кристаллы |
| Молярная масса | 85,10 г/моль |
| Плотность | 1,915 г/см³ |
| Температура | |
| • плавления | 387; 440; 441 |
| Растворимость | |
| • в воде | 2800; 413100 г/100 мл |
| • в этаноле | растворяется |
| Рег. номер CAS | 7758-09-0 |
| PubChem | 516910 |
| Рег. номер EINECS | 231-832-4 |
| SMILES |
N(=O)[O-].[K+]
|
| InChI |
1S/K.HNO2/c;2-1-3/h;(H,2,3)/q+1;/p-1
BXNHTSHTPBPRFX-UHFFFAOYSA-M
|
| Кодекс Алиментариус | E249 |
| RTECS | TT3750000 |
| ChemSpider | 22857 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Нитрит калия (азотистокислый калий) — калиевая соль азотистой кислоты с формулой KNO2. Представляет собой белый или слегка желтоватый кристаллический гигроскопический порошок. Очень хорошо растворим в воде. На воздухе медленно окисляется до нитрата калия КNO3. Пищевая добавка E249. Используется как улучшитель окраски и консервант в пищевой промышленности в изделиях из мяса и рыбы.
Содержание
Свойства
Нитрит калия образует бесцветные или слегка желтоватые высоко гигроскопичные кристаллы, моноклинной сингонии, пространственная группа I m, параметры ячейки a = 0,677 нм, b = 0,499 нм, c = 0,445 нм, β = 101,75°, Z = 2.
Очень хорошо растворим в воде, растворение сопровождается понижением температуры. Раствор имеет слабо щелочную реакцию из-за гидролиза по аниону.
Кристаллы разрушаются при 360 °C (до достижения точки плавления которая равна 440 °C или 441 °C, при 100 КПа по данным польской и английской Википедии и 438 °C при давлении в 101325 Па, энтальпия плавления — 17 кДж/моль).
Выше этой температуры разлагается по схеме:
-
- 4KNO2 ⟶ 2K2O + 2N2 + 3O2
Как и Нитрит натрия является окислителем особенно при повышенных температурах и реагирует с металлами такими как алюминий (особенно в порошкообразной форме), обезвоженными соединениями аммония такими как Сульфат аммония, цианидами и многими органическими соединениями.
На воздухе медленно доокисляется до нитрата калия KNO3:
-
- 2KNO2 + O2 ⟶ 2KNO3
Нитриты можно выявить по характеристической реакции с сульфатом железа (II) в присутствии концентрированной серной кислоты (по образованию коричневого окрашивания).
Нахождение в природе и способы получения
В природе, нитриты появляются на промежуточных этапах азотного цикла — как при нитрификации (присоединении азота к соединениям) так и при денитрификации (отсоединении азота от соединений). В промышленности Нитрит калия получают при реакции оксидов азота с гидроксидом калия.
Получается при окислении свинца нитратом калия:
-
- KNO3 + Pb ⟶ KNO2 + PbO
или в процессе термического разложения:
-
- 2KNO3 ⟶ 2KNO2 + O2
Применение
- Нитрит калия как пищевая добавка E249 (консервант) используется аналогично другим нитритам и солям (хлоридом натрия и нитритом натрия) — предотвращает образование ботулотоксина (образуется при жизнедеятельности палочки Clostridium botulinum). При добавлении к мясу образует нитрозомиоглобин, имеющий характерный красный цвет, который можно наблюдать в большинстве продуктов питания (колбасы, сосиски, и др.). Употребление продуктов, содержащих Нитрит калия, вызывает жажду.
- В Европейском союзе продажа нитрита калия для пищевых целей разрешена только в виде смеси с пищевой солью, с содержанием нитрита около 0,6 %. C 2013 года сходные правила действуют в России.
- Нитрит калия применяется для диазотирования при производстве азо-красителей.
- Нитрит калия применяется в аналитической химии для распознавания аминов.
- Нитрит калия применяется в фотографии как сенсибилизатор.
Биологическое действие
Токсичен при проглатывании, при получении больших доз вызывает раздражение, цианоз, конвульсии, смерть (образует метгемоглобин). Раздражает кожу и глаза. Летальная доза LD50 для кроликов 200 мг/кг.
Поступление нитритов с пищей оценивается в 31-185 или 40-100 мг в день.
В питьевой воде, согласно требованиям ВОЗ 1970 и 2004 гг, допускается содержание нитритов не более 44-50 мг на литр.
Приемлемые уровни потребления нитритов для людей 3,7 — 7 мг / кг.
