Новости
Нефтегазовая пром.
01.04.2025
01.04.2025
01.04.2025
Выставки
Наука и технология
31.03.2025
31.03.2025
Теги
Хромат калия
Хромат калия
| Хромат калия | |
|---|---|
 |
|
| Систематическое наименование |
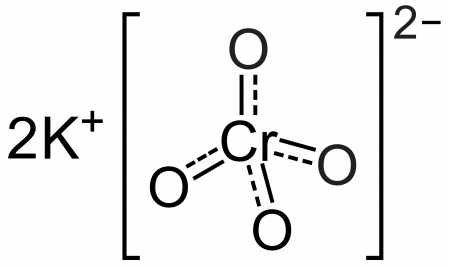
Хромат калия |
| Традиционные названия | Хромовокислый калий |
| Хим. формула | K2CrO4 |
| Состояние | жёлтые кристаллы |
| Молярная масса | 194,19 г/моль |
| Плотность | 2,732 г/см³ |
| Температура | |
| • плавления | 968,3; 973 °C |
| • кипения | 1000 °C[1] |
| Растворимость | |
| • в воде | 63,020; 75,180; 79,2100 г/100 мл |
| Показатель преломления | 1,74 |
| Рег. номер CAS | 7789-00-6 |
| PubChem | 24597 |
| Рег. номер EINECS | 232-140-5 |
| SMILES |
[O-][Cr](=O)(=O)[O-].[K+].[K+]
|
| InChI |
1S/Cr.2K.4O/q;2*+1;;;2*-1
XMXNVYPJWBTAHN-UHFFFAOYSA-N
|
| RTECS | GB2940000 |
| ChEBI | 75249 |
| ChemSpider | 22999 |
| Токсичность | яд и канцероген |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Хромат калия — неорганическое соединение, соль металла калия и хромовой кислоты с формулой K2CrO4, жёлтые кристаллы, растворимые в воде, окрашивает раствор, как и многие другие хроматы, в желтый цвет.
Содержание
Получение
- В природе встречается редкий минерал тарапакаит — Хромат калия с примесями.
- Окисление оксида хрома III хлоратом калия:
- Растворение оксида хрома VI в едком кали:
-
- CrO3 + 2KOH → K2CrO4 + H2O
- Разложение бихромата калия при нагревании:
-
- 4K2Cr2O7 →500−600oC 4K2CrO4 + 2Cr2O3 + 3O2
- Действие концентрированного раствора едкого кали на дихромат калия:
-
- K2Cr2O7 + 2KOH → 2K2CrO4 + H2O
![Хромат калия]()
Калий хромат и дихромат калия.
Физические свойства
Хромат калия образует жёлтые кристаллы ромбической сингонии, пространственная группа P nam, параметры ячейки a = 0,761 нм, b = 1,040 нм, c = 0,592 нм, Z = 4.
При 668°С переходит в гексагональную красную фазу.
Хорошо растворяется в воде с гидролизом по аниону. Плохо растворим в этаноле.
Химические свойства
- В разбавленных кислотах переходит в дихромат калия:
-
- 2K2CrO4 + 2HCl → K2Cr2O7 + 2KCl + H2O
- С концентрированными кислотами реакция идёт иначе:
-
- K2CrO4 + 2HCl → K[Cr(Cl)O3] + KCl + H2O
- С концентрированными горячими кислотами проявляются окислительные свойства:
-
- 2K2CrO4 + 16HCl →90oC 2CrCl3 + 3Cl2↑ + 4KCl + 8H2O
- Вступает в обменные реакции:
-
- K2CrO4 + 2AgNO3 → Ag2CrO4↓ + 2KNO3
- K2CrO4 + Hg2(NO3)2 → Hg2CrO4↓ + 2KNO3
Применение
- В качестве поглотителя УФ излучения лампы накачки в твердотельных лазерах для предотвращения деградации активной среды.
- Как протрава при крашении тканей.
- Окрашивание стекла в жёлтый цвет.
- Дубитель в кожевенной промышленности.
- Отбеливатель для масла и воска.
- Окислитель в органическом синтезе.
- Хромат калия используется как химический стандарт для калибровки калориметров по температуре и теплоемкости.
Токсичность
Хромат калия очень ядовит и канцерогенен, как и многие другие соединения шестивалентного хрома.

