Метасиликат натрия
Метасиликат натрия
| Метасиликат натрия | |
|---|---|
 |
|
| Систематическое наименование |
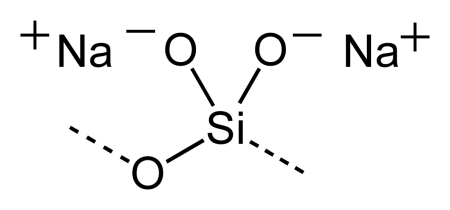
Метасиликат натрия; силикат натрия |
| Традиционные названия | Кремнекислый натрий |
| Хим. формула | Na2SiO3 |
| Состояние | бесцветные или белые кристаллы |
| Молярная масса | 122,06 г/моль |
| Плотность | 2,4; 2,61 г/см³ |
| Т. плав. | 1088; 1089 °C |
| Энтальпия образования | −1535 кДж/моль |
| Растворимость в воде | 18,820; 92,390 г/100 мл |
| Показатель преломления | 1,52 |
| ГОСТ | ГОСТ 13079-93 |
| Рег. номер CAS | 6834-92-0 |
| PubChem | 23266 |
| Рег. номер EINECS | 229-912-9 |
| SMILES |
[Na+].[Na+].[O-][Si]([O-])=O
|
| InChI |
1S/2Na.O3Si/c;;1-4(2)3/q2*+1;-2
NTHWMYGWWRZVTN-UHFFFAOYSA-N
|
| Рег. номер EC | 229-912-9 |
| RTECS | VV9275000 |
| ChEBI | 60720 |
| Номер ООН | 3253 |
| ChemSpider | 21758 |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Метасиликат натрия — неорганическое соединение, соль щелочного металла натрия и метакремниевой кислоты с формулой Na2SiO3, бесцветные или белые кристаллы, растворяется в холодной воде, образует кристаллогидрат.
Содержание
Получение
- Сплавление диоксида кремния с едким натром:
-
- SiO2 + 2NaOH →900−1000oC Na2SiO3 + H2O
- или карбонатом натрия:
-
- SiO2 + Na2CO3 →1150oC Na2SiO3 + CO2
- Разложение ортосиликата натрия:
-
- Na4SiO4 →1120oC Na2SiO3 + Na2O
- Безводную соль получают нагреванием кристаллогидрата:
-
- Na2SiO3 ⋅ 9H2O →100−300oC Na2SiO3 + 9H2O
Физические свойства
Метасиликат натрия образует бесцветные или белые кристаллы ромбической сингонии, пространственная группа C cm2, параметры ячейки a = 0,6078 нм, b = 1,053 нм, c = 0,4825 нм, Z = 4.
Хорошо растворим в холодной воде, концентрированные растворы образуют коллоидный раствор «жидкое стекло» гидрозоля SiO2•n H2O.
Из водных растворов выделяется кристаллогидрат Na2SiO3•9H2O, который плавится при 47°С в собственной кристаллизационной воде и начинает разлагаться при температуре выше 100°С.
Разлагается в горячей воде.
Водные растворы имеют щелочную реакцию из-за гидролиза по аниону.
Химические свойства
- Гидролизуется горячей водой:
-
- Na2SiO3 + (n + 1)H2O →T 2NaOH + SiO2↓ ⋅ nH2O
- Разлагается кислотами:
-
- Na2SiO3 + 2HCl → 2NaCl + SiO2↓ + H2O
- и щелочами:
-
- Na2SiO3 + 2NaOH → Na4SiO4 + H2O
- Реагирует с углекислым газом:
-
- Na2SiO3 + CO2 → Na2CO3 + SiO2↓
Применение
- Компонент шихты в производстве стекла.
- Производство жаростойких кислотоупорных бетонов.
- В качестве наполнителя в облегченных цементных растворах для цементирования скважин.
- Обеззараживание грубых поверхностей.

