Сульфит натрия
сульфит натрия
| сульфит натрия | |
|---|---|
 |
|
 |
|
| Хим. формула | Na2SO3 |
| Молярная масса | 126,037 г/моль |
| Плотность | 2,633 г/см³ |
| Т. плав. | 500 °C |
| Т. разл. | 600 °C |
| Растворимость в воде | 14,29 г/100 мл (0 °С) 26,10 г/100 мл (20 °С) 36,99 г/100 мл (40 °С) 29,20 г/100 мл (80 °С) |
| ГОСТ | ГОСТ 195-77 ГОСТ 5644-75 ГОСТ 903-76 |
| Рег. номер CAS | 7757-83-7 |
| PubChem | 24437 |
| Рег. номер EINECS | 231-821-4 |
| SMILES |
[O-]S(=O)[O-].[Na+].[Na+]
|
| InChI |
1S/2Na.H2O3S/c;;1-4(2)3/h;;(H2,1,2,3)/q2*+1;/p-2
GEHJYWRUCIMESM-UHFFFAOYSA-L
|
| Кодекс Алиментариус | E221 |
| RTECS | WE2150000 |
| ChEBI | 86477 |
| ChemSpider | 22845 |
| Токсичность | умеренная |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
сульфит натрия (сернистокислый натрий) — неорганическое соединение, соль натрия и сернистой кислоты с формулой Na2SO3. Применяют в фотографии, при изготовлении тканей и вискозного волокна, при обработке руд цветных металлов и для обезвреживания сточных вод.
Содержание
- 1 История
- 2 Физические свойства
- 3 Химические свойства
- 3.1 Фотографические свойства
- 3.1.1 Антиоксидант
- 3.1.2 Разрыв цепи полимеризации
- 3.1.3 Обесцвечивающий агент
- 3.1.4 Поддержание активности проявления
- 3.1 Фотографические свойства
- 4 Получение
- 5 Применение
- 6 Безопасность

История
В фотографии впервые было использовано в 1882 году Х. Б. Беркли для пирогаллоловых проявителей с целью уменьшить пятна, возникающие на фотоматериале в процессе обработки. С 1882 года многие составы включали в себя сульфитные ионы, как правило с целями защиты проявителя от окисления, но в целом роль этих ионов была малопонятна и только спустя годы исследований удалось выявить значительный ряд функций этого соединения в составе проявляющих растворов.
Физические свойства
Соединение имеет вид бесцветных кристаллов гексагональной сингонии с параметрами: a=0,5459 нм, с=0,6160 нм, z=2, пространственная группа C3. Плотность 2,633 г/см3. Растворим в воде, при этом с ростом температуры растворимость сначала растет (в 100 г воды): 14,29 г (при 0 °C), 26,10 г (при 20 °C), 36,99 г (при 40 °C), дальше падает: 29,20 г (при 80 °C). Предел температуры, после которой начинается уменьшение растворимости и начало кристаллизации — 33,4 °C.
Образует гептагидрат Na2SO3·7H2O при кристаллизации из водных растворов ниже 33,4 °C. Гептагидрат сульфита натрия имеет плотность 1,539 г/см3.
Химические свойства
сульфит натрия устойчив на воздухе при комнатной температуре, но при нагревании разлагается с образованием сульфата натрия и сульфида натрия, при этом при температуре выше 800 °C разложение идет до образования оксида натрия и диоксида серы.
Гептагидрат сульфита натрия во влажном воздухе легко окисляется до сульфата натрия, для замедления окисления используют ингибиторы — Гидрохинон, пирогаллол, 1,4-фенилендиамин. В сухом воздухе гептагидрат не окисляется, но частично теряет кристаллизационную воду, полностью обезвоживаясь при температуре 150—160 °C.
Водные растворы сульфита натрия имеют щелочную реакцию, при их подкислении происходит выделение диоксида серы.
сульфит натрия является сильным восстановителем. В водных растворах находится в частично гидролизованном состоянии, легко окисляется кислородом воздуха, перманганатом калия, бихроматом калия, бромом, иодом и другими окислителями до сульфата натрия. Растворы сульфита натрия поглощают диоксид серы, образуя гидросульфит натрия, а при кипячении присоединяют серу с образованием тиосульфата натрия. В кислых растворах хлорида титана (III), двуххлористого олова и хлорида железа (II) восстанавливается до дитионита натрия или до сульфида натрия.
Фотографические свойства
Многочисленные исследования свойств сульфита натрия в составе проявляющих растворов показали, что действие этого соединения не ограничивается узкой областью снижения количества пятен на эмульсии, образующихся в процессе обработки в некоторых окрашивающих проявителях, для чего это соединение было предложено изначально. Практически сразу сульфит натрия стал использоваться в своей роли основного универсального сохраняющего вещества, что было вызвано его многоаспектным действием на фотографические составы при всех этапах проявления и хранения растворов.
Антиоксидант
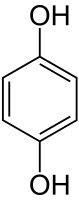
Основная роль сульфита натрия в составе фотографических проявляющих растворов заключается в защите органических проявляющих веществ от окисления кислородом воздуха. При высоком значении pH раствора проявляющее вещество в отсутствии сульфита быстро окисляется, становясь фотографически неактивным. Например, Гидрохинон сначала превращается в хинон, вследствие чего раствор приобретает жёлтую окраску, а затем в фотографически неактивный оксихинон, окрашивающий раствор в тёмно-коричневый цвет. Небольшое количество сульфита натрия резко замедляет этот процесс за счет того, что вместо гидрохинона с кислородом в первую очередь будет реагировать сам сульфит с образованием сульфата натрия. Присутствие же органического проявляющего вещества, в свою очередь, является ингибитором процесса окисления сульфита кислородом.
Точный механизм ингибирования окисления органических проявляющих веществ неизвестен, но предполагается, что он обусловлен связыванием сульфитом натрия окрашенных окисленных форм проявляющих веществ, которые в несвязанном состоянии катализируют дальнейшее окисление своей неокисленной формы.
Окисление гидрохинона кислородом воздуха в растворах, содержащих сульфит натрия, будет происходить уже не с образованием хинона и оксихинона, а с образованием бесцветного добезилата натрия, который также является проявляющим веществом:
-
![сульфит натрия]() + O2 + 2 Na2SO3 →H2O
+ O2 + 2 Na2SO3 →H2O ![сульфит натрия]() + Na2SO4 + NaOH
+ Na2SO4 + NaOH
Разрыв цепи полимеризации
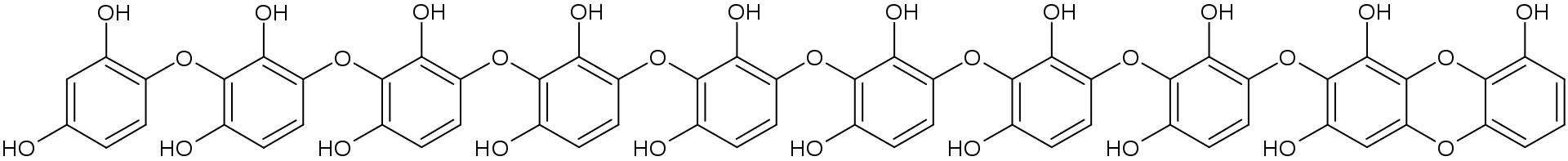
При проявлении гидрохиноном и его производными в растворе образуются семихиноны — высокоактивные и нестабильные соединения. Они имеют тенденцию к полимеризации в гуминовые кислоты, цепи которых в типичных условиях для фотографического проявления образуются из порядка 10 молекул окисленных остатков гидрохинона и имеют тёмную окраску. Так как на стадии образования семихинона сульфит реагирует с ним, то полимеризации, как правило, не происходит, а следовательно, не будет и каталитического воздействия данных полимерных соединений на неокисленную форму проявляющего вещества. Тем не менее, для пирогаллола сульфит не способен взаимодействовать с нерастворимыми окрашенными продуктами окисления, аналогично и для слабоокрашенных продуктов окисления фенидона и L-аскорбиновой кислоты.
Обесцвечивающий агент
сульфит натрия в описанном выше процессе связывания окрашенных форм образует бесцветные соединения, вместо сильноокрашенных, тем самым снижая нежелательные пятна и окраску результирующего изображения.
Поддержание активности проявления
Окисленные остатки проявляющего вещества в растворе, хотя и непосредственно не реагируют с галогенидом серебра в эмульсии, но изменяют pH среды и другие её показатели, что может вести либо к нарастанию скорости проявления, либо к её спаду. Лишь немногие проявляющие вещества не дают подобного эффекта. Рост активности наблюдается в проработавших растворах проявляющих веществ, имеющих активные гидроксогруппы, например у глицина-фото. Если же проявляющее вещество имеет только аминогруппы, то скорость проявления будет падать. Превращение окисленных форм в сульфонаты при реакции с сульфитом стабилизирует и поддерживает активность, тем самым позволяя избегнуть нежелательного пере- или недопроявления.
Получение
сульфит натрия получают:
- взаимодействием растворов Na2CO3 с SO2:
-
- Na2CO3 + SO2 → Na2SO3 + CO2
- нейтрализацией раствора NaHSO3 раствором гидроксида натрия при 38—40 °C с последующим охлаждением и кристаллизацией гептагидрата.
-
- NaHSO3 + NaOH → Na2SO3 + H2O
- реакцией гидроксида натрия и диоксида серы:
-
- 2NaOH + SO2 → Na2SO3 + H2O
Безводную соль:
- выделяют кристаллизацией при 95—100 °C или обезвоживанием гептагидрата;
- получают реакцией NaHSO3 с Ca(ОН)2:
-
- 2NaHSO3 + Ca(OH)2 ⟶ CaSO3↓ + Na2SO3 + 2H2O
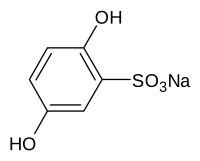
- получают как побочный продукт при производстве фенола из бензолсульфокислоты.
Применение
Применяют для удаления следов хлора после отбеливания тканей, для удаления серы из вискозного волокна после формования, как флотореагент для руд цветных металлов, в производстве пестицидов, для обезвреживания сточных вод, содержащих хром.
В фотографии используют как основное сохраняющее вещество в проявителях, входит в состав фиксажей и других растворов.
Безопасность
Временно допустимая концентрация в воздухе 0,1 мг/м3.