Тиосульфат аммония
Тиосульфат аммония
| Тиосульфат аммония | |
|---|---|
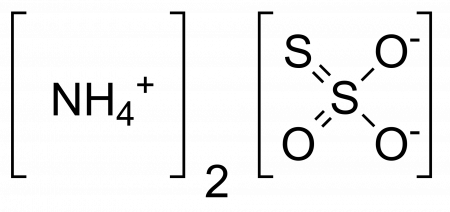 |
|
| Систематическое наименование |
Тиосульфат аммония |
| Традиционные названия | Тиосернокислый аммоний |
| Хим. формула | (NH4)2SO3S |
| Состояние | бесцветные кристаллы |
| Молярная масса | 148,21 г/моль |
| Плотность | 1,68 г/см³ |
| Температура | |
| • плавления | разл. 150 °C |
| Растворимость | |
| • в воде | 103,3100 г/100 мл |
| Рег. номер CAS | 7783-18-8 |
| PubChem | 6096946 |
| Рег. номер EINECS | 231-982-0 |
| SMILES |
[O-]S([O-])(=O)=S.[NH4+].[NH4+]
|
| InChI |
1S/2H3N.H2O3S2/c;;1-5(2,3)4/h2*1H3;(H2,1,2,3,4)
XYXNTHIYBIDHGM-UHFFFAOYSA-N
|
| ChemSpider | 4807475 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Тиосульфат аммония (гипосульфит аммония, аммоний серноватистокислый) — неорганическое соединение, соль аммония и тиосерной кислоты с формулой (NH4)2SO3S, бесцветные кристаллы, растворимые в воде. Применяется в фотографии как основной компонент быстрых фиксажей.
Содержание
Получение
- Медленная реакция суспензии серы с раствором гидрата аммония:
-
- 4 (NH3 ⋅ H2O) + 4 S → (NH4)2SO3S + 2 NH4HS + H2O
- Медленное окисление на воздухе гидросульфида аммония:
-
- NH4HS →−NH3 O2 S,(NH4)2Sn, (NH4)2SO3S
- Слияние горячих растворов гидросульфида аммония и гидросульфита аммония:
-
- 2 NH4HS + 4 NH4HSO3 →80oC 3 (NH4)2SO3S + 3 H2O
Физические свойства
Тиосульфат аммония образует бесцветные кристаллы с запахом аммиака, хорошо растворимые в воде, слабо растворимые в ацетоне, не растворяются в этаноле.
Химические свойства
- Разлагается при нагревании с образованием смеси продуктов:
-
- (NH4)2SO3S →150oC (NH4)2SO4, NH3, H2S
- Медленно разлагается в разбавленных растворах:
-
- (NH4)2SO3S →τ (NH4)2SO3 + S ↓
- Разлагается концентрированными кислотами:
-
- (NH4)2SO3S + 2 HCl → 2 NH4Cl + SO2 ↑ + S ↓ + H2O
- и горячими разбавленными кислотами:
-
- (NH4)2SO3S + 2 HCl + H2O →100oC 2 NH4Cl + H2SO4 + H2S ↑
- Реагирует с галогенами:
-
- (NH4)2SO3S + 4 Cl2 + 5 H2O → 2 NH4Cl + 2 H2SO4 + 8 HCl
Как и Тиосульфат натрия, реагирует с галогенидами серебра, образуя растворимые комплексы, что позволяет осуществлять процесс фиксирования при обработке фотографических материалов. В отличие от тиосульфата натрия, который позволяет достигать концентрации 6 г. серебра на литр раствора, Тиосульфат аммония позволяет почти удвоить это количество, снижая тем самым расход реактивов. Процесс фиксирования также происходит значительно быстрее (на 50 % для некоторых эмульсий), чем для фиксажей с тиосульфатом натрия.
Однако слишком длительная обработка в фиксажах приводит к растворению металлического серебра в областях низкой плотности и потере деталей на изображении. Эффект особенно сильно выражен на мелкозернистых эмульсиях и быстрых фиксажах на тиосульфате аммония (из-за их большей активности), что требует точного соблюдения температурно-временно́го регламента процесса обработки. Также, для уменьшения этого эффекта, быстрые фиксажи применяются в различных степенях разбавления для плёнок и для фотобумаг; при этом для фотобумаг, имеющих более мелкозернистую эмульсию, требуется применять примерно в два раза более сильное разбавление.
Применение
Используется как компонент фиксирующих растворов в фотографии вместо тиосульфата натрия для ускорения процесса фиксирования. Так как имеет плохую сохранность в кристаллической форме, то часто непосредственно перед применением для этой цели его готовят в растворе, смешивая Тиосульфат натрия с хлоридом аммония.
