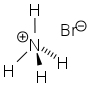
Бромид аммония
Бромид аммония
| Бромид аммония | |||
|---|---|---|---|
|
|||
| Систематическое наименование |
Бромид аммония | ||
| Традиционные названия | Бромистый аммоний | ||
| Хим. формула | NH4Br | ||
| Состояние | бесцветные кристаллы | ||
| Молярная масса | 97,943 г/моль | ||
| Плотность | 2,429 г/см³ | ||
| Температура | |||
| • разложения | 394°C | ||
| Растворимость | |||
| • в воде | 59,50; 74,220; 119,380; 134,7100 г/100 мл | ||
| Показатель преломления | 1,712 | ||
| Рег. номер CAS | 12124-97-9 | ||
| PubChem | 25514 | ||
| Рег. номер EINECS | 235-183-8 | ||
| SMILES |
[Br-].[NH4+]
|
||
| InChI |
1S/BrH.H3N/h1H;1H3
SWLVFNYSXGMGBS-UHFFFAOYSA-N
|
||
| RTECS | BO9155000 | ||
| ChEBI | 85364 | ||
| ChemSpider | 23804 | ||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Бромид аммония — неорганическое соединение, соль аммония и бромистоводородной кислоты с формулой NH4Br, бесцветные кристаллы, растворимые в воде. При нагревании сублимируется и разлагается. Устойчив на свету и на воздухе (при полном отсутствии примесей). Хорошо растворяется в воде (гидролиз по катиону). Не образует кристаллогидратов.
Содержание
Получение
- Растворение аммиака в бромистоводородной кислоте:
-
- NH3 + HBr → NH4Br
- Восстановление брома в концентрированном растворе аммиака:
-
- 8 NH3 + 3 Br2 → N2 ↑ + 6 NH4Br
- Разложение карбоната аммония бромистоводородной кислотой:
-
- (NH4) 2 CO3 + 2 HBr → 2 NH4Br + CO2 ↑ + H2O
![Бромид аммония]()
Физические свойства
Бромид аммония образует бесцветные кристаллы (β-модификация) кубической сингонии, пространственная группа P m3m, параметры ячейки a = 0,406 нм, Z = 1.
При нагревании происходит фазовый переход в α-модификацию кубической сингонии, пространственная группа F m3m, параметры ячейки a = 0,691 нм, Z = 4 (250°С).
При низких температурах существует γ-модификация — тетрагональная сингония, пространственная группа P 4b2, параметры ячейки a = 0,4248 нм, c = 0,4035 нм, Z = 1.
Хорошо растворяется в воде, этаноле, ацетоне, эфире.
Водные растворы имеют слабокислую реакцию из-за гидролиза.
Химические свойства
- При нагревании выше 394 °C возгоняется с разложением:
-
- NH4Br ⇄ NH3 + HBr
- Разлагается разбавленными кислотами:
-
- 2 NH4Br + H2SO4 → (NH4)2SO4 + 2 HBr ↑
- Окисляется концентрированной серной кислотой (ω>50%, гор.):
-
- 2 NH4Br + 3 H2SO4 → 2 NH4HSO4 + Br2 + SO2 ↑ + 2 H2O
- Разлагается щелочами:
- Концентрированный горячий раствор реагирует с магнием:
-
- 2 NH4Br + Mg → MgBr2 + H2 ↑ + 2 NH3 ↑
- Является слабым восстановителем:
Применение
- Лекарственные препараты.
- Антипирен.