Новости
Нефтегазовая пром.
01.04.2025
Выставки
Наука и технология
31.03.2025
01.04.2025
31.03.2025
Теги
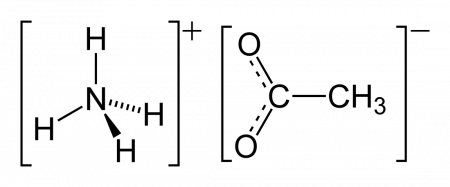
Ацетат аммония
Ацетат аммония
| Ацетат аммония | |
|---|---|
 |
|
| Систематическое наименование |
Ацетат аммония |
| Хим. формула | C2H7NO2 |
| Рац. формула | CH3COONH4 |
| Состояние | кристаллическое |
| Молярная масса | 77,0825 г/моль |
| Плотность | 1,07 г/см³ |
| Температура | |
| • разложения | 112 °C |
| Растворимость | |
| • в воде | 148 г/100 мл |
| Кристаллическая структура | ромбическая сингония |
| Рег. номер CAS | 631-61-8 |
| PubChem | 12432 |
| Рег. номер EINECS | 211-162-9 |
| SMILES |
CC(=O)O.N
|
| InChI |
1S/C2H4O2.H3N/c1-2(3)4;/h1H3,(H,3,4);1H3
USFZMSVCRYTOJT-UHFFFAOYSA-N
|
| Кодекс Алиментариус | E264 |
| RTECS | AF3675000 |
| ChEBI | 62947 |
| ChemSpider | 11925 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Ацетат аммония — аммониевая соль уксусной кислоты. Пищевая добавка E264 (консервант).
Содержание
Получение
Ацетат аммония получают по реакциям:
CH3CN + 2H2O = CH3COONH4
CH3COOH + NH3 = CH3COONH4
Химические свойства
При сравнительно низкой температуре 112 °C (385 K) разлагается на воду и ацетамид:
NH4C2H3O2 → CH3C(O)NH2 + H2O
В водном растворе подвергается гидролизу:
CH3COONH4 + HOH ↔ NH4OH + CH3COOH
Применение
Соль слабой кислоты и слабого основания, Ацетат аммония применяется:
- как биоразлагаемый реагент — антиобледенитель
- как буфер совместно с раствором уксусной кислоты. Особенностью данного буфера является его разложение при низких температурах без образования ионов.
- в органическом синтезе: реакция Кнёвенагеля.
- Растворенный в дистиллированной воде используется как коагулянт, осаждающий белки из раствора.


