Оксид меди (I)
Оксид меди (I)
| Оксид меди (I) | |
|---|---|
 |
|
| Традиционные названия | Закись меди, гемиоксид меди, оксид димеди |
| Хим. формула | Cu2O |
| Рац. формула | Cu2O |
| Внешний вид | Коричнево-красные кристаллы |
| Молярная масса | 143,09 г/моль |
| Плотность | 6,1 г/см³ |
| Твёрдость | 3,5 — 4 |
| Энтальпия | |
| • плавления | +64,22 кДж/моль |
| Растворимость | |
| • в воде | 2,4⋅10−7 г/100 мл |
| Показатель преломления | 2,85 |
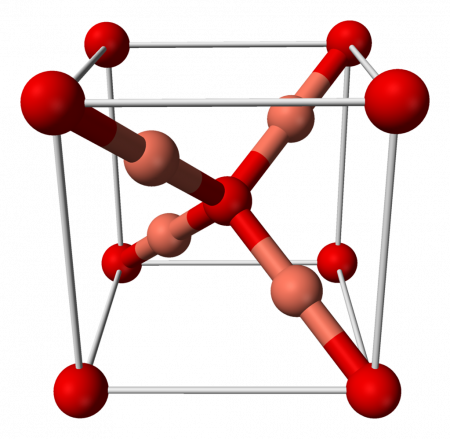
| Кристаллическая структура | кубическая |
| Рег. номер CAS | 1317-39-1 |
| PubChem | 10313194 |
| Рег. номер EINECS | 215-270-7 |
| SMILES |
[Cu]O[Cu]
|
| InChI |
1S/2Cu.O/q2*+1;-2
KRFJLUBVMFXRPN-UHFFFAOYSA-N
|
| RTECS | GL8050000 |
| ChEBI | 81908 |
| ChemSpider | 8488659 |
| ЛД50 | 470 мг/кг |
| Токсичность | средняя |
| Пиктограммы СГС |   |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Оксид меди (I) (гемиоксид меди, окси́д димеди, устар. Закись меди) — химическое соединение с формулой Cu2O. Соединение меди с кислородом, основный оксид. Кристаллическое вещество коричнево-красного цвета. В природе встречается в виде минерала куприта.
Содержание
- 1 Нахождение в природе
- 2 Физические свойства
- 3 Химические свойства
- 4 Получение
- 5 Применение
- 6 Токсичность

Нахождение в природе
Оксид меди (I) встречается в природе в виде минерала куприта (устаревшие названия: красная медная руда, стекловатая медная руда, рубиновая медь). Цвет минерала красный, коричнево-красный, пурпурно-красный или чёрный. Твёрдость по шкале Мооса 3,5 — 4.
Разновидность куприта с удлиненными нитевидными кристаллами называется халькотрихит (устаревшее название: плюшевая медная руда). Кирпично-красная смесь куприта с лимонитом носит название «черепичная руда».
Физические свойства
Оксид меди (I) при нормальных условиях — твёрдое вещество коричнево-красного цвета нерастворимое в воде и этаноле. Плавится без разложения при 1242 °C.
Оксид меди (I) имеет кубическую сингонию кристаллической решётки, пространственная группа P n3m, a = 0,4270 нм, Z = 2.
Химические свойства
Реакции в водных растворах
Оксид меди (I) не реагирует с водой. В очень малой степени (ПР = 1,2⋅10−15) диссоциирует:
- Cu2O + H2O ⇄ 2Cu+ + 2OH−
Равновесие диспропорционирования:
- 2Cu+ ⇄ Cu2+ + Cu
Оксид меди (I) переводится в раствор:
- концентрированной соляной кислотой
- Cu2O + 4HCl ⟶ 2H[CuCl2] + H2O
- концентрированной щёлочью (частично)
- Cu2O + 2OH− + H2O ⇄ 2[Cu(OH)2]−
- концентрированным гидратом аммиака и концентрированными растворами солей аммония
- Cu2O + 4(NH3 ⋅ H2O) ⟶ 2[Cu(NH3)2]OH + 3H2O
- Cu2O + 2NH4+ ⟶ 2[Cu(H2O)(NH3)]+
- путём окисления до солей меди (II) различными окислителями (например, концентрированными азотной и серной кислотами, кислородом в разбавленной соляной кислоте)
- Cu2O + 6HNO3 ⟶ 2Cu(NO3)2 + 2NO2↑ + 3H2O
- Cu2O + 3H2SO4 ⟶ 2CuSO4 + SO2↑ + 3H2O
- 2Cu2O + 8HCl + O2 ⟶ 4CuCl2 + 4H2O
Также Оксид меди (I) вступает в водных растворах в следующие реакции:
- медленно окисляется кислородом до гидроксида меди (II)
- 2Cu2O + 4H2O + O2 ⟶ 4Cu(OH)2↓
- реагирует с разбавленными галогенводородными кислотами с образованием соответствующих галогенидов меди (I):
- Cu2O + 2HHal ⟶ 2CuHal↓ + H2O (Hal = Cl, Br, I)
- в разбавленной серной кислоте дисмутирует на сульфат меди (II) и металлическую медь
- Cu2O + H2SO4 ⟶ CuSO4 + Cu↓ + H2O
- восстанавливается до металлической меди типичными восстановителями, например гидросульфитом натрия в концентрированном растворе
- 2Cu2O + 2NaHSO3 ⟶ 4Cu↓ + Na2SO4 + H2SO4
Реакции при высоких температурах
Оксид меди (I) восстанавливается до металлической меди в следующих реакциях:
- при нагревании до 1800 °C (разложение)
- 2Cu2O →1800∘C 4Cu + O2
- при нагревании в токе водорода, монооксида углерода, с алюминием
- Cu2O + H2 →>250∘C 2Cu + H2O
- Cu2O + CO →250−300∘C 2Cu + CO2
- 3Cu2O + 2Al →1000∘C 6Cu + Al2O3
- при нагревании с серой
- 2Cu2O + 3S →>600∘C 2Cu2S + SO2
- 2Cu2O + Cu2S →1200−1300∘C 6Cu + SO2
Оксид меди (I) может быть окислен до соединений меди (II) в токе кислорода или хлора:
- 2Cu2O + O2 →500∘C 4CuO
- Cu2O + Cl2 →250∘C Cu2Cl2O
Также, при высоких температурах Оксид меди (I) реагирует:
- с аммиаком (образуется Нитрид меди (I) )
- 3Cu2O + 2NH3 →250∘C 2Cu3N + 3H2O
- c оксидами щелочных металлов и бария (образуются двойные оксиды)
- Cu2O + M2O →600−800∘C 2MCuO
- Cu2O + BaO →500−600∘C BaCu2O2
Прочие реакции
Оксид меди (I) реагирует с азидоводородом:
- при охлаждении выпадает осадок азида меди (II)
- Cu2O + 5HN3 →10−15∘C 2Cu(N3)2↓ + H2O + NH3↑ + N2↑
- при комнатной температуре в токе азидоводородной кислоты выпадает осадок азида меди (I)
- Cu2O + 2HN3 →20−25∘C 2CuN3↓ + H2O
Получение
Оксид меди (I) может быть получен:
- нагреванием металлической меди при недостатке кислорода
- 4Cu + O2 →>200∘C 2Cu2O
- нагреванием металлической меди в токе оксида азота (I) или оксида азота (II)
- 2Cu + N2O →500−600∘C Cu2O + N2
- 4Cu + 2NO →500−600∘C 2Cu2O + N2
- нагреванием металлической меди с оксидом меди (II)
- Cu + CuO →1000−1200∘C Cu2O
- термическим разложением оксида меди (II)
- 4CuO →1026−1100∘C 2Cu2O + O2
- нагреванием сульфида меди (I) в токе кислорода
- 2Cu2S + 3O2 →1200−1300∘C 2Cu2O + 2SO2
В лабораторных условиях Оксид меди (I) может быть получен восстановлением гидроксида меди (II) (например, гидразином):
- 4Cu(OH)2 + N2H4 ⋅ H2O →100∘C 2Cu2O ↓ + N2↑ + 7H2O
Также, Оксид меди(I) образуется в реакциях ионного обмена солей меди (I) с щелочами, например:
- в реакции йодида меди (I) с горячим концентрированным раствором гидроксида калия
- 2CuI + 2KOH ⟶ Cu2O↓ + 2KI + H2O
- в реакции дихлорокупрата (I) водорода с разбавленным раствором гидроксида натрия
- 2H[CuCl2] + 4NaOH ⟶ Cu2O↓ + 4NaCl + 3H2O
В двух последних реакциях не образуется соединения с составом, соответствующим формуле CuOH (гидроксид меди (I) ). Образование оксида меди (I) происходит через промежуточную гидратную форму переменного состава Cu2O ⋅ xH2O.
- Окисление альдегидов гидроксидом меди (II). Если к голубому осадку гидроксида меди (II) прилить раствор альдегида и смесь нагреть , то сначала появляется жёлтый осадок гидроксида меди (I):
-
- R−CHO + 2Cu(OH)2 →t R−COOH + 2CuOH↓ + H2O
- при дальнейшем нагревании желтого осадка гидроксида меди (I) превращается в красный Оксид меди (I):
- 2CuOH →tCu2O + H2O
Применение
Оксид меди (I) применяется как пигмент для окрашивания стекла, керамики, глазурей; как компонент красок, защищающих подводную часть судна от обрастания; в качестве фунгицида.
Обладает полупроводниковыми свойствами, используется в меднозакисных вентилях.
Токсичность
Оксид меди (I) — умеренно токсичное вещество: LD50 470 мг/кг (для крыс перорально). Вызывает раздражение глаз, может вызывать раздражение кожи и дыхательных путей.
Очень токсично для водной среды: LC50 для Daphnia magna составляет 0,5 мг/л в течение 48 ч.
