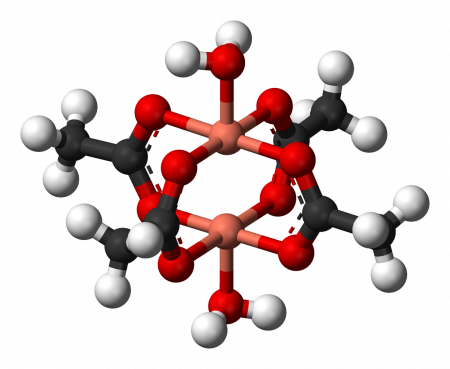
Ацетат меди (II)
Ацетат меди (II)
| Ацетат меди (II) | |
|---|---|
| Систематическое наименование |
Ацетат меди (II) |
| Традиционные названия | Уксуснокислая медь |
| Хим. формула | C4H6CuO4 и Cu2(CH3CO2)4(H2O)2 |
| Рац. формула | (CH3CoO)2Cu |
| Состояние | твёрдое |
| Молярная масса | 181.65(безводный) 199.67(моногидрат) г/моль |
| Плотность | 1.882 г/см³ |
| Температура | |
| • плавления | 115 °C |
| • кипения | 240 °C |
| • разложения | 290 °C |
| Растворимость | |
| • в воде | 7.2\20(холодная\горячая Вода) |
| • в этаноле | растворим |
| • в ацетоне | малорастворим (0.28г на 100г при 15°С) |
| Рег. номер CAS | 142-71-2 |
| PubChem | 8895 |
| Рег. номер EINECS | 205-553-3 |
| SMILES |
CC(=O)[O-].CC(=O)[O-].[Cu+2]
|
| InChI |
1S/2C2H4O2.Cu/c2*1-2(3)4;/h2*1H3,(H,3,4);/q;;+2/p-2
OPQARKPSCNTWTJ-UHFFFAOYSA-L
|
| ChemSpider | 8555 и 21169880 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Ацетат меди (II) (ярь-медянка; (CH3CoO)2Cu) — сложное химическое соединение, медная соль уксусной кислоты.
Содержание
- 1 Физические свойства
- 2 Получение
- 3 Химические свойства
- 3.1 Диссоциация
- 3.2 Реакции обмена
- 3.3 Реакции замещения
- 4 Применение
- 6 Фото
Физические свойства
Ацетат меди (II) представляет собой тёмно-сине-зелёные кристаллы моноклинной сингонии, растворимые в воде (7,1 г/100г воды), растворим также в спиртах, эфире.
Ацетат меди не горит, но окрашивает пламя в нежно-салатовый цвет.
Получение
Ацетат меди (II) получают взаимодействием гидроксида меди (II) c уксусной кислотой:
- Cu(OH)2 + 2CH3COOH ⟶ (CH3CoO)2Cu + 2H2O
Карбоната меди(II) c уксусной кислотой:
- CuCO3 + 2CH3COOH ⟶ (CH3CoO)2Cu + H2O + CO2↑
Так же можно получить смешиванием сульфата меди (II) c гидрокарбонатом натрия, и затем, после промывания осадка основного карбоната меди от сульфата натрия, добавить уксусной кислоты:
- 2CuSO4 + 4NaHCO3 ⟶ (CuOH)2CO3↓ + 2Na2SO4 + 3CO2↑ + H2O
- Cu2CO3(OH)2 + 4CH3COOH ⟶ 2(CH3CoO)2Cu + CO2↑ + 3H2O
Практически получается и растворением опилок металлической меди в уксусной эссенции при доступе кислорода воздуха. Процесс происходит медленно и на дне ёмкости по мере реакции вырастают крупные ровные кристаллы:
- 2Cu + O2 ⟶ 2CuO
- CuO + 2CH3COOH ⟶ (CH3COO)2Cu + H2O
Химические свойства
Диссоциация
Как и все растворимые соли, ацетат меди в водных растворах диссоциирует.
-
- (CH3COO)2Cu → 2CH3CoO− + Cu2+
Реакции обмена
Ацетат меди реагирует с сильными основаниями с образованием студенистого голубого осадка гидроксида меди (II) и соответствующей соли-ацетата.
-
- (CH3COO)2Cu + 2NaOH → Cu(OH)2↓ + 2CH3COONa
- Cu2+ + 2OH− → Cu(OH)2↓
Реакции замещения
Ацетат меди реагирует с металлами, стоящими левее меди в электрохимическом ряду активности металлов.
-
- (CH3COO)2Cu + Zn → (CH3CoO)2Zn + Cu↓
Применение
Моногидрат ацетата меди (II) (CH3CoO)2Cu·H2O — фунгицид, пигмент для керамики, реагент для обнаружения углеводов и селективно — глюкозы, катализатор полимеризации (стирола и др.), стабилизатор искусственных волокон.