Бромид меди (I)
Бромид меди (I)
| Бромид меди (I) | |
|---|---|
 |
|
| Систематическое наименование |
Бромид меди (I) |
| Традиционные названия | Бромистая медь |
| Хим. формула | CuBr |
| Состояние | твёрдое |
| Молярная масса | 143,45 г/моль |
| Плотность | 4,72 г/см³ |
| Температура | |
| • плавления | 504 °C |
| • кипения | 1350 °C |
| Мол. теплоёмк. | 71,9 Дж/(моль·К) |
| Энтальпия | |
| • образования | в газовой фазе: 120 кДж/моль; в твёрдой фазе: −105 кДж/моль |
| Растворимость | |
| • в воде | 1,2⋅10−3 г/100 мл |
| Показатель преломления | 2,09 |
| Рег. номер CAS | 7787-70-4 |
| PubChem | 24593 |
| Рег. номер EINECS | 232-131-6 |
| SMILES |
[Cu]Br
|
| InChI |
1S/BrH.Cu/h1H;/q;+1/p-1
NKNDPYCGAZPOFS-UHFFFAOYSA-M
|
| ChemSpider | 22995 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Бромид меди (I) — неорганическое вещество с формулой CuBr, соединение меди и брома. Относится к классу бинарных соединений, может рассматриваться как соль одновалентной меди и бромоводородной кислоты. В чистом виде — белое кристаллическое вещество, примеси бромида меди (II) окрашивают его в зеленоватый цвет.
Содержание
Физические свойства
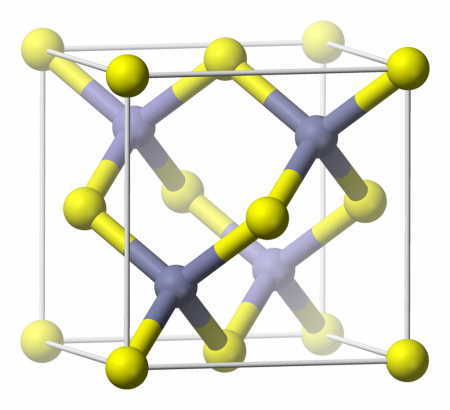
В чистом виде представляет собой бесцветные тетраэдрические микрокристаллы. Кристаллическая решётка типа сфалерита (кубическая сингония).
Во влажном воздухе на свету медленно окисляется, приобретая зеленоватый цвет. Термически устойчив: плавится и кипит без разложения. Нерастворим в воде, этаноле, эфире. Не образует кристаллогидраты.
Химические свойства
Образование растворимых соединений
Бромид меди (I) растворяется в горячей концентрированной серной кислоте:
- 2CuBr + 4H2SO4 ⟶ 2CuSO4 + Br2↑ + 2SO2↑ + 4H2O
За счёт комплексообразования растворяется в концентрированных растворах бромоводородной кислоты, бромида калия, цианида калия, аммиака:
- CuBr + 2KCN ⟶ K[Cu(CN)2] + KBr
- CuBr + 2(NH3 ⋅ H2O) ⟶ [Cu(NH3)2]Br + 2H2O
Прочие реакции
При кипячении водной суспензии бромида меди (I) происходит дисмутация последнего на бромид меди (II) и металлическую медь:
- 2CuBr ⟶ Cu↓ + CuBr2
Бромид меди(I) медленно окисляется на свету во влажном воздухе:
- 4CuBr + O2 + 2H2O ⟶ 4CuBr(OH)
Образует молекулярные аддукты с основаниями Льюиса, например с диметилсульфидом:
Получение
Бромид меди (I) можно получить одним из следующих способов.
Термическим разложением бромида меди (II):
- 2CuBr2 →>500∘C 2CuBr + Br2
- 2(CuBr2 ⋅ 4H2O) →115−140∘C 2CuBr + Br2 + 8H2O
Реакцией оксида меди (I) с разбавленной бромоводородной кислотой:
- 2Cu2O + 2HBr ⟶ 2CuBr↓ + H2O
Восстановлением растворимых солей двухвалентной меди диоксидом серы в присутствии растворимых бромидов, например:
- 2CuSO4 + 2NaBr + SO2 + 2H2O ⟶ 2CuBr↓ + 2H2SO4 + Na2SO4
Пропусканием газообразного бромоводорода через суспензию металлической меди в эфире с последующим разложением образовавшегося дибромокупрата (I) водорода:
- 2Cu + 4HBr ⟶ 2H[CuBr2] + H2↑
Восстановлением растворимых солей двухвалентной меди металлической медью в присутствии бромида калия с последующим разложением образовавшегося дибромокупрата (I) калия:
- CuSO4 + 4KBr + Cu ⟶ 2K[CuBr2] + K2SO4
Применение
Бромид меди (I) применяется в органическом синтезе.
