Сульфид меди (I)
Сульфид меди (I)
| Сульфид меди (I) | |
|---|---|
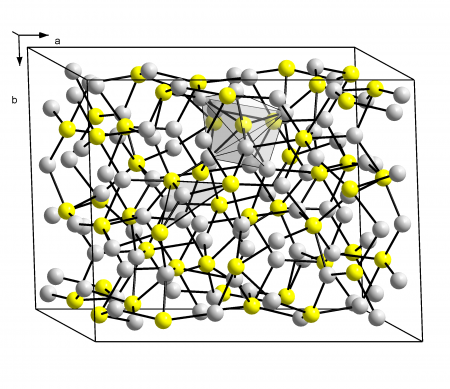 Кристаллическая структура халькозина |
|
| Систематическое название | Моносульфид димеди |
| Другие названия | Сульфид меди (I) |
| Химическая формула | Cu2S |
| Эмпирическая формула | Cu2−XS, x = 0÷0,10 |
| Внешний вид | твердое вещество темно-серого цвета |
| Молярная масса | 159,16 г/моль |
| Температура плавления | 1129 °C (1402,15 К) |
| Температура разложения | 700 °C (в вакууме) |
| Фазовые переходы | 103 °C (ромб. → гекс.) 437 °C (гекс. → куб.) |
| Плотность | 5,81 г/см³ |
| Твёрдость по Моосу | 2,5÷3,0 |
| Растворимость в воде | 1,3⋅10−15 г/100 мл |
| Произведение растворимости | 2,3⋅10−48 |
| ПДК | в воздухе 4 мг/м3 |
| Кристаллическая решётка | Орторомбическая |
| Стандартная энтальпия образования | −79 кДж/моль |
| Энтальпия плавления | +23,01 кДж/моль |
| Стандартная молярная энтропия | +121 Дж/(моль·К) |
| Стандартная энергия образования Гиббса | −86 кДж/моль |
| Регистрационный номер CAS | 22205-45-4 |
| Регистрационный номер EC | 244-842-9 |
| Где это не указано, данные приведены при стандартных условиях (25 °C, 100 кПа). | |
Сульфид меди (I) — неорганическое вещество с формулой Cu2S. Относится к классу бинарных соединений. Может также рассматриваться как соль одновалентной меди и сероводородной кислоты.
Содержание
Нахождение в природе
Сульфид меди(I) в природе встречается в виде минерала халькозина (устаревшие названия: халькоцит, редрутит, медный блеск). Также, по составу данному соединению близок минерал джюрлеит, иногда называют джарлеит (подробнее см. Сульфиды меди). Основные свойства представлены в таблице.
| Халькозин | Джюрлеит | |
|---|---|---|
| Состав | Cu2S | Cu1,94S |
| Цвет | темно-серый | чёрный |
| Сингония | ромбическая | моноклинная |
| Плотность, г/см³ | 5,5—5,8 | 5,5—5,7 |
| Твердость | 2,5—3,0 | 2,2—2,4 |
Физические свойства
Сульфид меди (I) — твердое вещество темно-серого цвета, нерастворимое в воде и этаноле.
Cu2S существует в трёх кристаллических модификациях:
- α-Cu2S, ромбическая сингония, пространственная группа Ab 2m, параметры ячейки a = 1,1190 нм, b = 2,728 нм, c = 1,341 нм, Z = 96, d = 5,81 г/см3;
- β-Cu2S, гексагональная сингония, пространственная группа P 63/mmc, параметры ячейки a = 0,389 нм, c = 0,668 нм, Z = 2, d = 5,78 г/см3;
- γ-Cu2S, кубическая сингония, пространственная группа F m3m, параметры ячейки a = 0,5735 нм, Z = 4, d = 5,60 г/см3.
Температуры фазовых переходов: α → β 103 °C, β → γ 437 °C.
Сульфид меди (I) склонен к образованию нестехиометрических соединений, свойства которых могут сильно отличаться от стехиометрических.
Химические свойства
Реакции при высоких температурах
При атмосферном давлении в инертной атмосфере:
- Cu2S →1000−1130∘C Cu2−x S + xCu
В вакууме:
- Cu2S →>700∘C 2Cu + S
С водяным паром:
- Cu2S + 2H2O →>600∘C 2Cu + SO2 + 2H2
С кислородом:
- 8Cu2S + 15O2 →500−600∘C 6Cu2O + 4CuSO4 + 4SO2
- 2Cu2S + 3O2 →1200−1300∘C 2Cu2O + 2SO2
- Cu2S + 2Cu2O →1200−1300∘C 6Cu + SO2
С хлором:
- Cu2S + Cl2 →300−400∘C 2CuCl + S
С сульфидом железа(II) и серой:
- Cu2S + 2FeS + S →800−1000∘C 2(FeIII CuI)S2
- 2(FeIIICuI)S2 + 5O2 + 2SiO2 →1000∘C 2Cu + 2FeSiO3 + 4SO2
Реакции в растворах
Сульфид меди (I) не реагирует с соляной кислотой.
Растворяется в горячей концентрированной азотной кислоте, концентрированном растворе цианида калия:
- Cu2S + 12HNO3 ⟶ Cu(NO3)2 + CuSO4 + 10NO2↑ + 6H2O
- Cu2S + 4KCN ⟶ 2K[Cu(CN)2] + K2S
Медленно растворяется в холодной концентрированной азотной кислоте, горячей концентрированной серной кислоте, концентрированном растворе аммиака:
- Cu2S + 8HNO3 ⟶ 2Cu(NO3)2 + S↓ + 4NO2↑ + 4H2O
- Cu2S + 6H2SO4 ⟶ 2CuSO4 + 5SO2 ↑ + 6H2O
- Cu2S + 4(NH3 ⋅ H2O) ⟶ [Cu(NH3)2]2S + 4H2O
Восстанавливает Fe3+ до Fe2+ (в растворе):
- Cu2S + 4Fe(p)3+ →80∘C 2 Cu(p)2+ + 4Fe(p)2+ + S↓
- Cu2S + 2Fe(p)3+ →20∘C CuS↓ + Cu(p)2+ + 2Fe(p)2+
Получение
Сульфид меди (I) может быть получен одним из следующих способов.
Нагреванием металлической меди с серой в вакууме:
- 2Cu + S →300−400∘C Cu2S
Нагреванием металлической меди в токе диоксида серы:
- 4Cu + SO2 →600−800∘C Cu2S + 2CuO
Термическим разложением сульфида меди (II):
- 2CuS →200−450∘CCu2S + S
Нагреванием сульфида меди (II) в токе водорода:
- 2CuS + H2 →600−700∘CCu2S + H2S
Нагреванием оксида меди(I) с серой:
- 2Cu2O + 3S →>600∘C 2Cu2S + SO2
Монокристаллы сульфида меди (I) получают при помощи зонной плавки.
Применение
Руды, содержащие Сульфид меди (I) — один из видов сырья для производства меди, медного купороса. Сульфид меди (I) — компонент медного штейна при пирометаллургическом получении меди. Также используется как полупроводник, компонент полупроводниковых сплавов.
Влияние на здоровье
Пыль сульфида меди (I) токсична, ПДК в воздухе 4 мг/м³.
