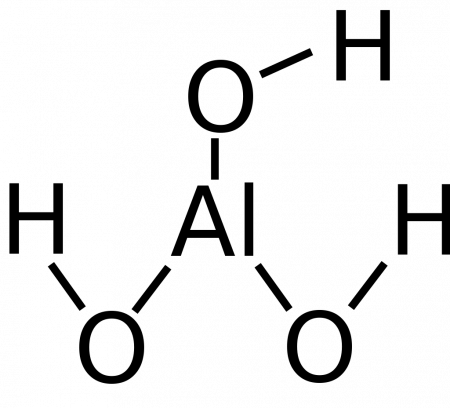
Гидроксид алюминия
Гидроксид алюминия
| Хим. формула | AlH₃O₃ |
| Номер CAS | 21645-51-2 |
| PubChem | 10176082 |
| ChemSpider | 8351587 |
| Номер EINECS | 244-492-7 |
| RTECS | BD0940000 |
| ChEBI | 33130 |
| DrugBank | DB06723 |
| Приводятся данные для стандартных условий (25 ℃, 100 кПа), если не указано иное. | |
Гидроксид алюминия — вещество с формулой Al(OH)3 (а также H3AlO3) — соединение оксида алюминия с водой. Белое студенистое вещество, плохо растворимое в воде, обладает амфотерными свойствами.
Содержание
- 1 Получение
- 2 Физические свойства
- 3 Химические свойства
- 4 Безопасность
- 4.1 ЛД50
- 5 Применение
Получение
Al(OH)3 получают при взаимодействии солей алюминия с водными растворами щёлочи, избегая их избытка:
AlCl3 + 3 NaOH ⟶ Al(OH)3 ↓ + 3 NaCl
Гидроксид алюминия выпадает в виде белого студенистого осадка.
Второй способ получения гидроксида алюминия — взаимодействие водорастворимых солей алюминия с растворами карбонатов щелочных металлов:
-
- 2 AlCl3 + 3 Na2CO3 + 3 H2O → 2 Al(OH)3 ↓ + 6 NaCl + 3 CO2
Физические свойства
Гидроксид алюминия представляет собой белое кристаллическое вещество, для которого известны 4 кристаллические модификации:
- моноклинный (γ) гиббсит
- триклинный (γ') гиббсит (гидрагилит)
- байерит (γ)
- нордстрандит (β)
Существует также аморфный Гидроксид алюминия переменного состава Al2O3•nH2O
Химические свойства
Свежеосаждённый Гидроксид алюминия может взаимодействовать с:
- кислотами
- Al(OH)3 + 3 HCl ⟶ AlCl3 + 3 H2O
- Al(OH)3 + 3 HNO3 ⟶ Al(NO3)3 + 3 H2O
- щелочами
- В концентрированном растворе гидроксида натрия:
- Al(OH)3 + NaOH ⟶ Na[Al(OH)4]
- При сплавлении твёрдых реагентов:
- Al(OH)3 + NaOH →1000oC NaAlO2 + 2 H2O
При нагревании разлагается:
-
- 2 Al(OH)3 →t>575oC Al2O3 + 3 H2O
С растворами аммиака не реагирует.
Безопасность
ЛД50
>5000 мг/кг (крысы, перорально).
Применение
Гидроксид алюминия используется при очистке воды, так как обладает способностью адсорбировать различные вещества.
В медицине, в качестве антацидного средства, в качестве адъюванта при изготовлении вакцин.
В качестве абразивного компонента зубной пасты.
В качестве антипирена (подавителя горения) в пластиках и других материалах.
После обработки до окислов применяется в качестве носителя для катализаторов.