Нитрат ртути I
Нитрат ртути I
| Нитрат ртути I | |
|---|---|
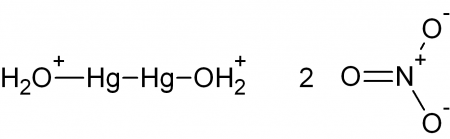 |
|
| Систематическое наименование |
Нитрат ртути I |
| Хим. формула | Hg2(NO3)2 |
| Состояние | бесцветные кристаллы |
| Молярная масса | 525.2 г/моль |
| Плотность | 4,79 г/см³ |
| Температура | |
| • плавления | 70 °C |
| Энтальпия | |
| • образования | -868 кДж/моль |
| Рег. номер CAS | [7782-86-7] |
| PubChem | 51346573 |
| Рег. номер EINECS | 233-886-4 |
| SMILES |
[N+](=O)([O-])O[Hg].[N+](=O)([O-])O[Hg].O.O
|
| InChI |
1S/2Hg.2NO3.2H2O/c;;2*2-1(3)4;;/h;;;;2*1H2/q2*+1;2*-1;;
LSABZDVKJBWCBE-UHFFFAOYSA-N
|
| ChemSpider | 9493944 и 21493988 |
| Токсичность | Чрезвычайно токсичен |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Нитрат ртути I — химическое соединение, существует только в виде димера Hg2(NO3)2.
Синонимы: динитрат диртути, Ртуть азотнокислая закисная.
Физические и химические свойства
В чистом виде — бесцветные кристаллы, в воде гидролизуются, растворимы в сероуглероде и азотной кислоте. Растворы обладают сильными восстановительными свойствами. Для предотвращения частичного окисления кислородом воздуха, в растворы нитрата ртути добавляют свободную ртуть.
Образует кристаллогидрат Hg2(NO3)2•2H2O. На воздухе теряет кристаллогидратную воду.
Неустойчив, при добавлении щелочи к раствору соли образуется чёрный осадок:
Разлагается при температуре 70-150°C:
- Hg2(NO3)2 → 2 HgO + 2 NO2
Концентрированный раствор соли гидролизуется водой с образованием осадка основной соли:
- Hg2(NO3)2 + H2O → Hg2NO3(OH) ↓ + HNO3
Реагирует с разбавленной хлороводородной кислотой:
- Hg2(NO3)2 + 2 HCl → Hg2Cl2 ↓ + 2 HNO3
Окисляется горячей концентрированной азотной кислотой:
- Hg2(NO3)2 + 4 HNO3 → 2 Hg(NO3)2 + 2 NO2 ↑ + 2 H2O
Может также окислиться разбавленной азотной кислотой в присутствии кислорода:
- 2 Hg2(NO3)2 + 4 HNO3 + O2 → 4 Hg(NO3)2 + 2 H2O
Выпадение желтого осадка ртути при реакции с медью:
- Hg2(NO3)2 + C u → 2 H g ↓ + C u ( N O 3 ) 2
Реагирует с насыщенным раствором сероводорода:
- Hg2(NO3)2 + H2S → HgS ↓ + Hg ↓ + 2 HNO3
Выпадает осадок дийодида диртути при добавлении йодида калия:
- Hg2(NO3)2 + 2 KI → Hg2I2 ↓ + 2 KNO3
На холоду реагирует с гидрокарбонатом калия:
- Hg2(NO3)2 + 2 KHCO3 → Hg2CO3 ↓ + 2 KNO3 + H2O + CO2 ↑
Получение
Соль может быть получена из металлической ртути при действии разбавленной азотной кислоты на холоду:
- 6 Hg + 8 HNO3 → 3 Hg2(NO3)2 + 2 NO ↑ + 4 H2O
А также при добавлении жидкой ртути к нитрату ртути:
- Hg(NO3)2 + Hg ⇄ Hg2(NO3)2
Производство
В СССР выпускался химический реактив Ртуть I азотнокислая 2-водная нескольких квалификаций по ГОСТ 4521-78.
Применение
- В химическом анализе в меркуриметрических методах объёмного анализа.
- Чернение латуни
- Компонент глазурей
- Компонент пиротехнических составов
Токсикология и физиологические свойства
Как и многие другие соединения ртути, Нитрат ртути I Hg2(NO3)2 (Ртуть азотнокислая, закисная, динитрат диртути, нитрат диртути 2+) - это очень токсичное вещество. Сильнейший неорганический яд. В высоких концентрациях вредно влияет на центральную нервную систему.


