Йодметан
Йодметан
| Йодметан | |||
|---|---|---|---|
|
|||
| Систематическое наименование |
Йодметан | ||
| Традиционные названия | метилйодид | ||
| Хим. формула | CH3I | ||
| Рац. формула | CH3I | ||
| Состояние | жидкость | ||
| Молярная масса | 141,94 г/моль | ||
| Плотность | 2,2789 г/см³ | ||
| Энергия ионизации | 9,54 ± 0,01 эВ | ||
| Температура | |||
| • плавления | -66,45 °C | ||
| • кипения | 42,43 °C | ||
| • вспышки | -28 °C | ||
| Давление пара | 50 атм | ||
| Растворимость | |||
| • в воде | 1,4 г/100 мл | ||
| Показатель преломления | 1,5304 | ||
| Дипольный момент | 1,59 Д | ||
| Рег. номер CAS | 74-88-4 | ||
| PubChem | 6328 | ||
| Рег. номер EINECS | 200-819-5 | ||
| SMILES |
CI
|
||
| InChI |
1S/CH3I/c1-2/h1H3
INQOMBQAUSQDDS-UHFFFAOYSA-N
|
||
| RTECS | PA9450000 | ||
| ChEBI | 39282 | ||
| Номер ООН | 2644 | ||
| ChemSpider | 6088 | ||
| Токсичность | токсичен, канцероген | ||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
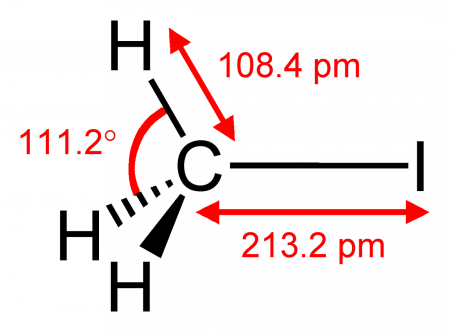
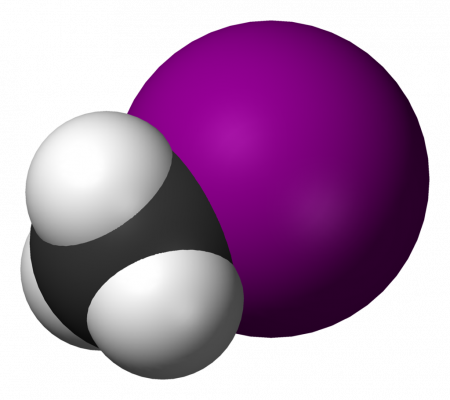
Йодметан (Йодистый метил, метилйодид, MeI) — органическое соединение с формулой CH3I, продукт замещения йодом одного из атомов водорода в молекуле метана. Тяжёлая летучая жидкость. Часто используется в органическом синтезе для метилирования. В природе выделяется в небольшом количестве рисом.
Содержание
- 1 Свойства
- 2 Получение
- 3 Применение
- 4 Безопасность
Свойства
Тяжёлая подвижная жидкость, желтеющая при стоянии, особенно на свету из-за выделения I2. Для предотвращения этого иодметан хранят в тёмной посуде над медной проволокой, поглощающей йод.
Получение
Получают по экзотермической реакции между метанолом и трийодидом фосфора, который получается in situ из красного фосфора:
- 3 CH3OH + PI3 → 3 CH3I + H3PO3
- или
- CH3OH + H3PO4 + KI → CH3I + KH2PO4 + H2O (3-4 ч. t под ОХ рефлюкс, перемешивание)
Также получают реакцией йодида калия с диметилсульфатом в присутствии карбоната кальция:
- (CH3)2SO4 + KI → K2SO4 + 2 CH3I
Для очистки CH3I может быть обработан Na2S2O3 для удаления йода. Очистку также можно осуществить обработкой раствором соды с последующей сушкой над плавленным хлористым кальцием и перегонкой.
Также его можно получить реакцией йодида калия с метилтозилатом:
- KI + CH3OSO2C6H4CH3 → CH3I + KOSO2C6H4CH3
Применение
Йодметан является отличным реагентом для реакций замещения SN2. Он стерически открыт для атак нуклеофилам, к тому же йод является хорошей уходящей группой. 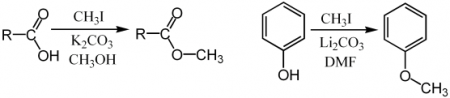
В представленных реакциях основные карбонаты K2CO3 или Li2CO3 удаляют кислые протоны, в результате чего образуются карбоксильный и фенольный карбанион, который выступает в роли нуклеофила в SN2 реакции. Йодиды являются более «мягкими» реагентами в нуклеофильных реакциях в силу более слабой связи с внешними электронами и более лёгкой поляризуемости йодида. В силу этого он предпочитает более «мягкие» нуклеофилы. Так, при алкилировании тиоционата происходит алкилирование по сере, а не по азоту с образованием CH3SCN, а не CH3NCS. Это также наблюдается при алкилировании 1,3-дикарбонильных соединений, метилирование енолятов этих соединений практически полностью идёт по углеродному атому, хотя заряд сосредоточен больше на атомах кислорода.
Йодметан легко образует метилмагнийиодид. Он широко распространён на практике из-за лёгкости получения и часто используется в учебных лабораториях. В процессе Monsanto Йодметан образуется in situ из метанола и йодоводорода. CH3I затем реагирует с окисью углерода в присутствии родиевых комплексов с образованием ацетилиодида, прекурсора уксусной кислоты после гидролиза. Большое количество уксусной кислоты получается таким способом.
Безопасность
Ярко выраженный канцероген. ЛД50 при ингаляции для крыс 76 мг/кг. В печени метилйодид быстро превращается в S-метилглутатион. Вдыхание большого количества паров йодметана вызывает поражение лёгких, печени, почек и центральной нервной системы, что приводит к тошноте, головокружению, кашлю и рвоте. Длительный контакт с кожей вызывает ожоги. Большие дозы при ингаляции вызывают отёк лёгких.
Пределы взрываемости воздушных смесей 8.5—66 %.