Фторид йода VII
Фторид йода VII
| Фторид йода VII | |||
|---|---|---|---|
|
|||
| Систематическое наименование |
Фторид йода VII | ||
| Хим. формула | IF7 | ||
| Рац. формула | IF7 | ||
| Молярная масса | 259,89 г/моль | ||
| Плотность | 2,7 г/см³ | ||
| Температура | |||
| • плавления | 4,5 °C | ||
| • кипения | 4,77 °C | ||
| • разложения | 350 °C | ||
| Растворимость | |||
| • в воде | реагирует | ||
| Рег. номер CAS | 16921-96-3 | ||
| PubChem | 85645 | ||
| Рег. номер EINECS | 240-981-4 | ||
| SMILES |
FI(F)(F)(F)(F)(F)F
|
||
| InChI |
1S/F7I/c1-8(2,3,4,5,6)7
XRURPHMPXJDCOO-UHFFFAOYSA-N
|
||
| ChemSpider | 21477354 | ||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Фторид йода VII (гептафторид йода), IF7 — бесцветный ядовитый тяжёлый (почти в 9 раз тяжелее воздуха) газ (при 20 °C), с резким неприятным запахом, высший фторид йода, в котором атом йода проявляет степень окисления +7.
Содержание
Физическо-химические свойства
До сегодняшнего дня нет единого мнения о температурах фазового перехода соединения, поскольку его сложно отчистить от примеси IOF5, который занижает температуру плавления. По некоторым данным, температура плавления соединения находится в пределах 6,4 ± 0,1°С.
| Свойство | Значение |
|---|---|
| Энтальпия образования (298 К, в газовой фазе) | −122,22 кДж/моль(по другим данным[3] −229,80 кДж/моль) |
| Энтропия образования (300 К, в газовой фазе) | 355,16 Дж/(моль·К) |
| Теплоёмкость (300 К, в газовой фазе) | 137,09 Дж/(моль·К) |
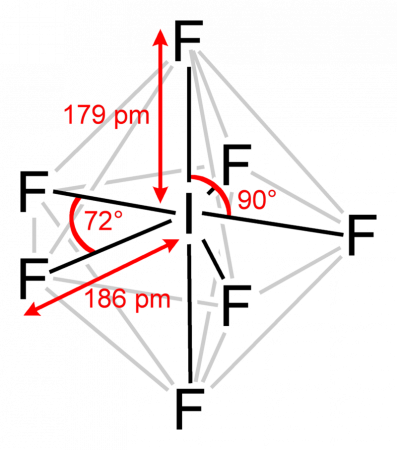
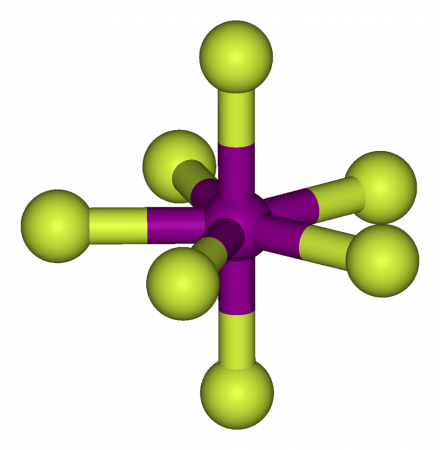
Строение
Пентагонально-бипирамидальное строение молекулы подтверждено спектроскопически при помощи ИК, КР и ЯМР-19F спектроскопии.
Методы получения
- Известен метод получения гептафторида взаимодействием йода с фторидами металлов, например, фторидом серебра. Такую реакцию впервые наблюдал Каммерер. Однако, в таких условиях также получается пентафторид йода:
- Также применяется метод получения из простых веществ. Для этого фтор пропускают над йодом в платиновом реакторе. Сначала образуется пентафторид йода, который при 270 °C реагирует с фтором и образуется гептафторид.
-
- I2 + 5 F2 → 2 IF5
- Чаще всего применяют взаимодействие пентафторида йода с фтором, при этом проходят процессы аналогичные второй стадии предыдущего метода.
- Продукт, полученный вышеописанными методами, всегда загрязнён примесью IOF5 за счёт гидролиза IF7. Поэтому, для получения чистого продукта можно применять метод взаимодействия фтора с сухими йодидами. Например:
-
- PdI2 + 9 F2 → 2 IF7 + PdF4
Химические свойства
Химические свойства гептафторида йода во многом схожи со свойствами трифторида хлора. Химически чрезвычайно активен и агрессивен к большинству материалов. Сильный окислитель.
- Достаточно часто, в начале реакции молекула гептафторида отщепляет 2 атома фтора, которые участвуют в дальнейшей реакции, а IF5 выделяется с продуктами:
- Углекислый газ сгорает в присутствии IF7 с образованием простого йода:
-
- 7 CO2 + 4 IF7 → 2 I2 + 7 CF4 + 7 O2
- Гидролизуется водой, при этом образуется ортойодная кислота и фтороводород:
-
- IF7 + 6 H2O → H5IO6 + 7 HF
- Реагирует с диоксидом кремния и стеклом с образованием оксопентафторида йода и тетрафторида кремния:
-
- 2 IF7 + SiO2 → SiF4 + 2 IOF5
- С некоторыми фторидами (AsF5, SbF5, BF3) образует комплексные соединения, которые вполне устойчивы до температуры около 140 °C. Предположительно, структура таких соединений ионная: IF6+•AsF6−.
- Органические соединения при контакте с гептафторидом йода воспламеняются или взрываются с образованием массы различных продуктов, которые обычно не полностью идентифицированы.
Применение
Нашёл некоторое применение в органическом синтезе.
Опасности
Гептафторид йода высокоопасен, очень сильно раздражает кожу и слизистые оболочки.