Гидроксид лития
гидроксид лития
| гидроксид лития | |
|---|---|
 |
|
| Систематическое наименование |
гидроксид лития |
| Хим. формула | LiOH |
| Рац. формула | LiOH |
| Состояние | твёрдое |
| Молярная масса | 23,94637 г/моль |
| Плотность | 1,46 (25 °C) |
| Т. плав. | 462 |
| Т. кип. | 925 °C |
| Т. разл. | 930 |
| Энтальпия образования | -487,2 кДж/моль |
| Растворимость в воде | 12,7 (0 °C) |
| ГОСТ | ГОСТ 8595-83 |
| Рег. номер CAS | 1310-65-2 |
| PubChem | 3939 |
| Рег. номер EINECS | 215-183-4 |
| SMILES |
[Li+].[OH-]
|
| InChI |
1S/Li.H2O/h;1H2/q+1;/p-1
WMFOQBRAJBCJND-UHFFFAOYSA-M
|
| RTECS | OJ6307070 |
| ChEBI | 33979 |
| Номер ООН | 2680 |
| ChemSpider | 3802 и 21170131 |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
гидроксид лития — неорганическое основание щелочного металла лития, имеющее формулу LiOH. Является сильным основанием, но наиболее слабым основанием среди щелочных металлов.
Содержание
Физические свойства
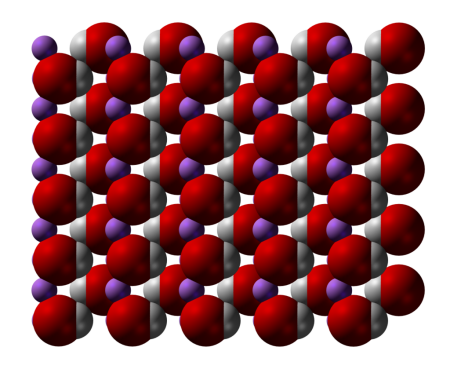
гидроксид лития при стандартных условиях представляет собой бесцветные кристаллы с тетрагональной решёткой. При работе с ним необходимо проявлять осторожность, избегать попадания на кожу и слизистые оболочки.
Растворяется в воде, 12,24 г/100 см3 при 25 °C, растворимость с температурой практически не повышается. В этаноле, в отличие от гидроксида натрия, почти не растворяется.
Получение
- Взаимодействие металлического лития с водой:
-
- 2Li + 2H2O ⟶ 2LiOH + H2↑
- Взаимодействие оксида лития с водой:
-
- Li2O + H2O ⟶ 2LiOH
- Взаимодействие карбоната лития с гидроксидом кальция:
-
- Li2CO3 + Ca(OH)2 ⟶ 2LiOH + CaCO3↓
- Обменными реакциями:
-
- Li2SO4 + Ba(OH)2 ⟶ 2LiOH + BaSO4↓
![Гидроксид лития]()
Химические свойства
- Взаимодействие с кислотами с образованием соли и воды (реакция нейтрализации):
- Взаимодействие с кислотными оксидами с образованием соли и воды:
- При нагревании в инертной атмосфере (Ar) разлагается:
-
- 2LiOH →800oC,A r Li2O + H2O
![Гидроксид лития]()
Применение
гидроксид лития используют для получения солей лития; как компонент электролитов в щелочных аккумуляторах и поглотитель углекислого газа в противогазах, подводных лодках и космических кораблях. Он также используется как катализатор полимеризации. Применяется в стекольной и керамической промышленности. При производстве водоупорных смазочных материалов, обладающих механической стабильностью в широком диапазоне температур.




