Нитрид лития
Нитрид лития
| Нитрид лития | |
|---|---|
 |
|
| Систематическое наименование |
Нитрид лития |
| Традиционные названия | Азотистый литий |
| Хим. формула | Li3N |
| Состояние | зеленовато-чёрные или тёмно-красные кристаллы |
| Молярная масса | 34,82 г/моль |
| Плотность | 1,28 г/см³ |
| Температура | |
| • плавления | 813, 845 °C |
| • кипения | разлагается °C |
| Мол. теплоёмк. | 75,2 Дж/(моль·К) |
| Энтальпия | |
| • образования | -164,0 кДж/моль |
| Рег. номер CAS | 26134-62-3 |
| PubChem | 520242 |
| Рег. номер EINECS | 247-475-2 |
| SMILES |
[Li+].[Li][N-][Li]
|
| InChI |
1S/3Li.H2N/h;;;1H2/q3*+1;-1
BHZCMUVGYXEBMY-UHFFFAOYSA-N
|
| ChEBI | 30525 |
| ChemSpider | 453793 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Нитрид лития — соединение щелочного металла лития и азота, зеленовато-чёрные или тёмно-красные кристаллы.
Единственный устойчивый нитрид щелочных металлов.
Применяется в пиротехнике.
Содержание
Получение
Синтезом из элементов — при комнатной температуре влажный азот медленно взаимодействует с литием, увеличение температуры и давления ускоряет реакцию:
- 6 Li + N2 →300oC 2 Li3N
Взаимодействием гидрида лития с азотом:
- 3 LiH + N2 →500oC Li3N + NH3
При хранении металлического лития в воздушной атмосфере при нормальных условиях наряду с карбонатом лития и гидроксидом лития в поверхностной плёнке образуется также Нитрид лития.
Физические свойства
Нитрид лития образует в зависимости от отклонения от стехиометрического состава зеленовато-чёрные или тёмно-красные кристаллы.
Нитрид лития эндотермическое соединение, энтальпия его образования из элементов −207 Нитрид лития кДж/моль.
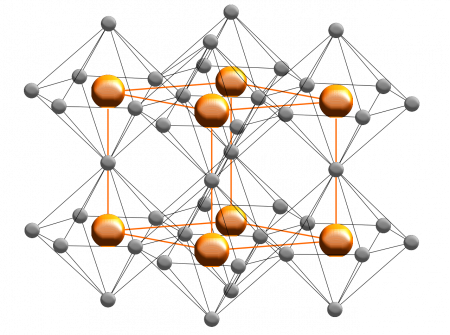
В нормальных условиях устойчива кристаллическая структура гексагональной сингонии, называемая α − Li3N, имеющая пространственная группу P 6/mmm, параметры кристаллической ячейки a = 0,3655 нм, c = 0,3876, Z = 1.
При давлении свыше 4200 бар (4 100 атм) α − Li3N переходит в β − Li3N, имеющий структуру арсенида натрия ( Na3As ). Пр повышении давления свыше 360 кбар β − Li3N переходит в γ − Li3N со структурой типа Li3Bi.
В кристалле α − Li3N атомы лития образуют гексагональную графитоподобную кристаллическую структуру, в одной из кристаллических плоскостей каждый атом азота окружён шестью атомами лития. Два дополнительных атома лития расположены в других соседних плоскостях над и под атомом азота и каждый атом азота в результате оказывается окружённым восемью атомами лития, расположенных в вершинах гексагональной бипирамиды.
Нитрид лития является твёрдым электролитом — обладает ионной электропроводимостью по ионам Li+ с удельной проводимостью 2·10-4 1/(Ом·см) и энергией активации освобождения ионов лития из узлов кристаллической решётки 0,26 эВ (~24 кДж/моль). Допирование кристалла водородом увеличивает проводимость, в то время как легирование ионами металлов (Al, Cu, Mg) уменьшает его. Установлено, что энергия активации межкристаллического переноса ионов лития выше чем внутрикристаллическая (~68,5 кДж/моль).
α − Li3N является полупроводником с шириной запрещенной зоны ~2,1 эВ.
Нитрид лития изучался как вещество для компактного хранения газообразного водорода, абсорбция и десорбция водорода обратимы и происходят при сравнительно низкой температуре ~270 °C. В опытах было достигнуто поглощение водорода веществом до 11,5 % по массе.
Химические свойства
Реакция образования нитрида лития обратима и при повышении температуры в вакууме идёт процесс разложения на элементы:
- 2 Li3N →400oC 6 Li + N2
Нитрид лития энергично взаимодействует с водой с образованием гидроксида лития и аммиака:
- Li3N + 3 H2O ⟶ 3 LiOH + NH3
Нитрид лития при повышенной температуре взаимодействует с водородом с образованием гидрида лития и аммиака:
- Li3N + 3 H2 ⟶ 3 LiH + NH3
При взаимодействии нитрида лития с водородом при 300 °C и повышенном давлении (более 0,5 МПа) образуется смесь гидрида лития и амида лития:
- Li3N + 2 H2 →300oC, 0.5 MPa LiNH2 + 2 LiH
Разлагается кислотами с образованием соответствующих кислоте солей лития и аммония:
Известно также много смешанных нитридов лития, некоторые из них: LiMgN , LiZnN , Li3AlN2, Li5SiN3, Li5TiN3, Li5GeN3
Расплавленный Нитрид лития агрессивен по отношению ко многим металлам (Fe, Cu, Ni, Pt и др.).
Применение
- Нитрид лития иногда используется как компонент при изготовлении пиротехнических смесей.
- Возможно применение вещества для компактного хранения водорода.