Хлорид бария
хлорид бария
| хлорид бария | |
|---|---|
 |
|
| Систематическое наименование |
хлорид бария |
| Традиционные названия | Хлористый барий |
| Хим. формула | BaCl2 |
| Рац. формула | BaCl2 |
| Состояние | твёрдое |
| Молярная масса | 208,246 г/моль |
| Плотность | 3,92 (20 °C) |
| Температура | |
| • плавления | 962 °C |
| • кипения | 1560 °C |
| Энтальпия | |
| • образования | -860,1 кДж/моль |
| Растворимость | |
| • в воде | 36,2 (20 °C) |
| ГОСТ | ГОСТ 4108-72 ГОСТ 742-78 |
| Рег. номер CAS | 10361-37-2 |
| PubChem | 25204 |
| Рег. номер EINECS | 233-788-1 |
| SMILES |
[Cl-].[Cl-].[Ba+2]
|
| InChI |
1S/Ba.2ClH/h;2*1H/q+2;;/p-2
WDIHJSXYQDMJHN-UHFFFAOYSA-L
|
| RTECS | CQ8750000 |
| ChEBI | 63317 |
| Номер ООН | 1564 |
| ChemSpider | 23540 |
| ЛД50 | 50-78 мг/кг (крысы, орально) |
| Пиктограммы ECB |   |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
хлорид бария (хлористый барий) — бинарное неорганическое вещество, относящееся к классу солей. Химическая формула — BaCl2.
Содержание

Описание
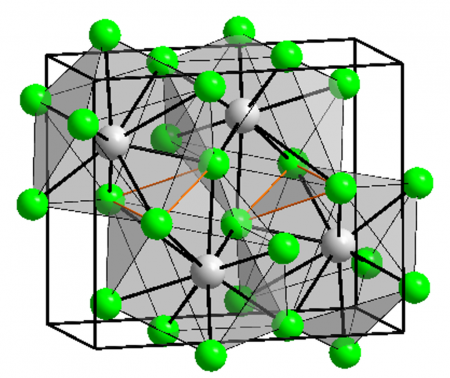
хлорид бария при стандартных условиях представляет собой бесцветные ромбические кристаллы. Малорастворим в спирте, не растворим в диэтиловом эфире. Из водных растворов кристаллизуется дигидрат хлорида бария BaCl2 ⋅ 2H2O — бесцветные кристаллы с моноклинной решёткой. Токсичен, ПДК 0,5 мг/м³
ГОСТ 4108-72 Реактивы. Барий хлорид 2-водный. Технические условия
Получение
1. Взаимодействие металлического бария с хлором:
Ba + Cl2 ⟶ BaCl2
2. Взаимодействие оксида бария с соляной кислотой:
BaO + 2HCl ⟶ BaCl2 + H2O
3. Взаимодействие гидроксида бария с соляной кислотой (реакция нейтрализации):
Ba(OH)2 + 2HCl ⟶ BaCl2 + 2H2O
4. Взаимодействие сульфида бария с хлоридом кальция:
BaS + CaCl2 ⟶ BaCl2 + CaS
5. Взаимодействие карбоната бария с соляной кислотой:
BaCO3 + 2HCl ⟶ BaCl2 + H2O + CO2↑
Химические свойства
1. Взаимодействие с растворами солей (реакция идёт, если образуется нерастворимое вещество):
BaCl2 + MgSO4 ⟶ BaSO4↓ + MgCl2
BaCl2 + K2CrO4 ⟶ BaCrO4↓ + 2KCl
2. Взаимодействие с некоторыми кислотами (реакция идёт, если образуется нерастворимое вещество):
BaCl2 + H2SO4 ⟶ BaSO4↓ + 2HCl
Применение
хлорид бария применяют в производстве пигментов (например, баритового жёлтого BaCrO4, касселевой зелени BaMnO4 и других соединений), в качестве добавки в электролиты при получении магния, для закалки быстрорежущей стали (в виде расплавов смеси хлорида бария с хлоридами щелочных и щёлочноземельных металлов), как компонент керамики, реактив на SO42− (сульфат-ион), для утяжеления и осветления кожи в кожевенной промышленности, как зооцид.
