Теллурид цинка
Теллурид цинка
| Теллурид цинка | |
|---|---|

Элементарная ячейка кристаллов типа цинковой обманки.
__ Zn __Te |
|
| Систематическое название | Теллурид цинка |
| Химическая формула | ZnTe |
| Внешний вид | красные кристаллы |
| Молярная масса | 193,01 г/моль |
| Температура плавления | 1564 ± 2 K; 1238,5 °C |
| Температура кипения | разл. |
| Плотность | 6,34 г/см³ |
| Твёрдость по Моосу | 3-4 |
| Теплопроводность | 0,18 Вт/(см*град) Вт/(м·K) |
| Кристаллическая решётка | кубическая, типа цинковой обманки, постоянная решётки 0,61 нм. Пространственная группа T2d-F43m |
| Координационное число | 4 |
| Структура молекулы | тетраэдрическая |
| Стандартная энтальпия образования | 109; 126 кДж/моль |
| Стандартная энергия образования Гиббса | 92; 79 кДж/моль*К |
| Регистрационный номер CAS | 1315-11-3 |
| PubChem | 3362486 |
| Где это не указано, данные приведены при стандартных условиях (25 °C, 100 кПа). | |
Теллурид цинка — бинарное соединение цинка и теллура с химической формулой ZnTe. Цинковая соль теллуроводородной кислоты. При нормальных условиях представляет собой твёрдое вещество. Полупроводник, обычно с дырочным типом проводимости и шириной запрещённой зоны 2,23—2,25 эВ.
Содержание
- 1 Свойства
- 2 Получение
- 3 Применение
- 3.1 Оптоэлектроника
- 3.2 Нелинейная оптика
- 4 Токсичность
Свойства
Физические свойства
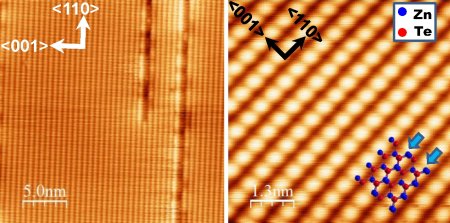
Представляет собой красновато-серый порошок, после очистки методом сублимации — рубиново-красные кристаллы. Устойчивая при стандартных условиях кристаллическая структура соединения кубическая, с кристаллической решёткой типа цинковой обманки (сфалерита). При испарении мощным световым излучением, в присутствии кислорода ZnTe кристаллизуется в виде гексагональных кристаллов типа вюрцита. Постоянная решётки кристаллической структуры типа сфалерита 0,61034 нм (расстояние между атомами Zn и Te 0,263 нм) и близка к постоянным решёток таких соединений как антимонид алюминия, антимонид галлия, арсенид индия и сульфид свинца(II), что позволяет выращивать монокристаллические малодислокационные плёнки ZnTe на подложках перечисленных соединений, или, наоборот, плёнки этих соединений на монокристаллической подложке ZnTe. Некоторые трудности представляет выращивание плёнок ZnTe на монокристаллической подложке арсенида галлия из-за различия постоянных решёток. Также, поликристаллические плёнки ZnTe с наноразмерными кристаллами можно выращивать на стеклянных подложках, например, при производстве фотогальванических солнечных элементов. В кристаллической структуре типа вюрцита ZnTe имеет постоянные решётки a = b = 0,427 нм и c = 0,699 нм.
Химические свойства
Не растворим в воде. Реагирует даже со слабыми кислотами с образованием теллуроводорода:
-
- ZnTe + 2HI → ZnI2 + H2Te↑
В газовой фазе при высокой температуре обратимо распадается на элементы, причём Te в газовой фазе присутствует в основном в виде молекул Te2:
-
- ZnTe ⇆ Zn + Te
Окисляется кислородом, в зависимости от условий окисления до оксида цинка и элементарного теллура или до оксида цинка и диоксида теллура:
-
- 2ZnTe + O2 → 2ZnO + 2Te
-
- 2ZnTe + 3O2 → 2ZnO + 2TeO2
Получение
Может быть получен разными способами:
- Синтезом из элементов. Производится длительным нагреванием смеси порошков Zn и Te в запаянной кварцевой ампуле:
-
- Zn + Te → ZnTe
- Взаимодействием растворимой соли цинка в водном растворе с теллуроводородом:
-
- ZnCl2 + H2Te → ZnTe↓ + 2HCl
- Обменной реакцией растворимого теллурида с растворимой солью цинка:
-
- Zn(NO3)2 + K2Te → ZnTe↓ + 2KNO3
- Электролитическим методом, при этом анод — цинковый и катод — теллуровый, в растворе кислоты, например, серной.
Применение
Оптоэлектроника
Так как ZnTe легко легируется акцепторными примесями, он является удобным материалом для применения в оптоэлектронике. Также используется для создания светодиодов с синим излучением, полупроводниковых лазеров, в солнечных элементах и в СВЧ-генераторах. В солнечных элементах может использоваться в качестве подслоя совместно с теллуридом кадмия. ZnTe, с p-типом проводимости используется в гетероструктурах Теллурид кадмия — Теллурид цинка в p-i-n диодах.
Также ZnTe является компонентом тройных полупроводниковых соединений (образует непрерывный ряд твёрдых растворов со структурой сфалерита с теллуридом ртути, сульфидом цинка и теллуридом кадмия). Например, Теллурид кадмия-цинка CdxZn(1-x)Te: при х = 0 отвечает соединению ZnTe, при х = 1 — соединению CdTe. Изменение параметра х позволяет оптимизировать спектральные оптические характеристики при применении в оптоэлектронике.
Нелинейная оптика
ZnTe и Ниобат лития часто используются для генерации электромагнитных импульсов терагерцевого диапазона для изучения свойств веществ методом импульсной терагерцевой спектроскопии и радиоволнового неразрушающего контроля диэлектрических деталей терагерцевым излучением. Генерация терагерцевого излучения в кристаллах ZnTe возбуждается высокоинтенсивными импульсами светового излучения и обусловлена нелинейными оптическими эффектами, приводящими к преобразованию энергии оптического излучения в энергию терагерцевых электромагнитных волн. И наоборот, облучение монокристалла ZnTe терагерцевым электромагнитным излучением вызывает в нём эффект двойного лучепреломления, изменяющий поляризацию проходящего света, что пригодно для создания детекторов терагерцевого излучения.
Легированный ванадием Теллурид цинка обладает ещё одном нелинейным оптическим свойством — изменять свой показатель преломления для оптического излучения под воздействием света (фоторефракция), что может быть применено для защиты приёмников видимого света от интенсивных его потоков. Ограничители излучения из этого материала лёгкие и компактные, в отличие от сложных оптических ограничителей и могут использоваться в качестве защитного средства оптических приёмников от обратимого «ослепления» интенсивным лазерным лучом, что позволяет после засветки лазером продолжать наблюдение слабоосвещённых картин. Также Теллурид цинка может быть использован в голографических интерферометрах в конфигурируемых оптических сетях и в качестве электрооптических модуляторов для коммутаторов световых потоков. По сравнению с дугими полупроводниками, (типов A[III]-B[V] или A[II]-B[VI]), ZnTe проявляет исключительно высокий эффект фоторефракции, причём его легирование марганцем существенно увеличивает этот эффект.
Токсичность
Считается высокотоксичным веществом, так как при взаимодействии с кислотами или горячей водой образуется чрезвычайно ядовитый теллуроводород.
|
Соединения цинка
|
|
|---|---|
|
|

