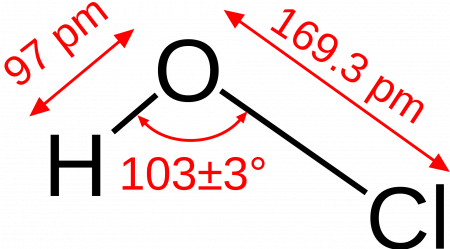
Хлорноватистая кислота
хлорноватистая кислота
| хлорноватистая кислота | |||
|---|---|---|---|
|
|||
| Систематическое наименование |
хлорноватистая кислота | ||
| Хим. формула | HClO | ||
| Состояние | бесцветный водный раствор | ||
| Молярная масса | 52.46 г/моль | ||
| Константа диссоциации кислоты pKa | 7.497 | ||
| Рег. номер CAS | 7790-92-3 | ||
| PubChem | 24341 | ||
| Рег. номер EINECS | 232-232-5 | ||
| SMILES |
OCl
|
||
| InChI |
1S/ClHO/c1-2/h2H
QWPPOHNGKGFGJK-UHFFFAOYSA-N
|
||
| ChEBI | 24757 | ||
| ChemSpider | 22757 | ||
| Пиктограммы ECB |   |
||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
хлорноватистая кислота — HClO, очень слабая одноосновная кислота, в которой хлор имеет степень окисления +1. Существует лишь в растворах.
Содержание
- 1 Свойства
- 2 Получение
- 3 Применение
Свойства
В водных растворах хлорноватистая кислота частично распадается на катион H+ и гипохлорит-анион ClO−
- HOCl ⇄ ClO− + H+
Неустойчива, постепенно разлагается даже в разбавленных водных растворах на хлороводород и атомарный Кислород, благодаря которому является сильным окислителем:
- HOCl → HCl + O
Реагирует с соляной кислотой HCl, образуя газообразный хлор:
- HOCl + HCl → H2O + Cl2
Как и хлорноватистая кислота, её соли — гипохлориты — являются сильными окислителями. Многие из них неустойчивы. Кристаллогидрат LiClO ⋅ H2O выдерживает длительное хранение; NaClO ⋅ H2O при 70 °C разлагается со взрывом, а KClO известен только в виде водных растворов. Ca(ClO)2 в сухом виде вполне устойчив, но в присутствии H2O и CO2 разлагается. Более стоек Mg(ClO)2.
Получение
хлорноватистая кислота получается при растворении хлора (реакция диспропорционирования) или оксида хлора(I) в воде.
В промышленном масштабе производятся гипохлориты кальция, натрия, калия, лития хлорированием известкового молока и соответствующих щелочей.
Применение
хлорноватистая кислота и гипохлориты легко разлагаются с выделением атомарного кислорода и поэтому широко используются для отбелки целлюлозы и тканей, а также для санитарных целей.