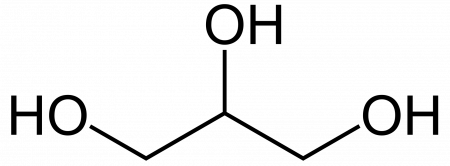
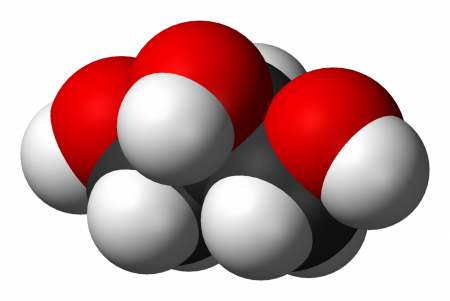
Глицерин
глицерин
| глицерин | |||
|---|---|---|---|
|
|||
 |
|||
| Традиционные названия | глицерин | ||
| Хим. формула | C3H8O3 | ||
| Рац. формула | HOCH2-CH(OH)-CH2OH | ||
| Молярная масса | 92,09 г/моль | ||
| Плотность | 1,261 г/см³ | ||
| Температура | |||
| • плавления | 17,9 °C | ||
| • кипения | 290 °C | ||
| • разложения | 554 ± 1 °F | ||
| • вспышки | 320 ± 1 °F и 160 °C | ||
| Давление пара | 0,003 ± 0,001 мм рт.ст. | ||
| Показатель преломления | 1,4740 | ||
| ГОСТ | ГОСТ 6824-96 ГОСТ 6823-2017 ГОСТ 6259-75 | ||
| Рег. номер CAS | 56-81-5 | ||
| PubChem | 753 | ||
| Рег. номер EINECS | 200-289-5 | ||
| SMILES |
OCC(O)CO
|
||
| InChI |
1S/C3H8O3/c4-1-3(6)2-5/h3-6H,1-2H2
PEDCQBHIVMGVHV-UHFFFAOYSA-N
|
||
| Кодекс Алиментариус | E422 | ||
| RTECS | MA8050000 | ||
| ChEBI | 17754 | ||
| ChemSpider | 733 | ||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
глицерин (от греч. γλυκερός — сладкий) — органическое соединение, простейший представитель трёхатомных спиртов с формулой C3H5(OH)3. Представляет собой вязкую прозрачную жидкость со сладким вкусом.
Синонимы: глицерóл, пропантриол-1,2,3.
Содержание
- 1 Физические свойства
- 2 Химические свойства
- 3 Получение
- 4 Производные глицерина и их место в обмене веществ живых организмов
- 4.1 Глицериды
- 5 Применение
Физические свойства
Бесцветная вязкая жидкость без запаха. Сладкий на вкус, отчего и получил своё название (греч. γλυκερός — сладкий). Имеет молярную массу 92,09 г/моль, относительную плотность d420 = 1,260, коэффициент преломления nD20 = 1,4740. Температура плавления составляет 17,9 °C, кипит при 290 °C, частично при этом разлагаясь. Гигроскопичен, поглощает воду из атмосферы в количестве до 40 % от собственной массы. С водой, метанолом, этанолом, ацетоном смешивается в любых пропорциях, но не растворим в эфире и хлороформе, хотя и способен растворяться в их смесях с этанолом.
При растворении глицерина в воде происходит выделение тепла и происходит контракция — уменьшение объёма раствора. Смеси глицерина с водой обладают температурой плавления значительно более низкой, чем каждое из веществ по отдельности, например, при массовом содержании глицерина в 66,7 % его смесь с водой будет замерзать при −46,5 °C.
Образует азеотропы с нафталином, его производными и рядом других веществ.
Химические свойства
Химические свойства глицерина типичны для многоатомных спиртов.
Взаимодействие глицерина с галогеноводородами или галогенидами фосфора ведёт к образованию моно- и дигалогенгидринов.
глицерин этерифицируется карбоновыми и минеральными кислородосодержащими кислотами с образованием соответствующих сложных эфиров. Так, с азотной кислотой глицерин образует тринитрат — нитроглицерин (получен в 1847 г. Асканио Собреро), использующийся в настоящее время в производстве бездымных порохов.
При дегидратации он образует токсичный акролеин:
-
- HOCH2CH(OH)−CH2OH ⟶ H2C = CH−CHO + 2H2O,
и окисляется до глицеринового альдегида CH2OHCHOHCHO, дигидроксиацетона CH2OHCOCH2OH или глицериновой кислоты CH2OHCHOHCOOH.
Сложные эфиры глицерина и высших карбоновых кислот — жиры являются важными метаболитами, важное биологическое значение играют также фосфолипиды — смешанные глицериды фосфорной и карбоновых кислот.
Получение
глицерин впервые был получен в 1779 году Карлом Вильгельмом Шееле при омылении жиров в присутствии оксидов свинца. Основную массу глицерина получают как побочный продукт при омылении жиров.
Большинство синтетических методов получения глицерина основано на использовании пропилена в качестве исходного продукта. Хлорированием пропилена при 450—500 °С получают аллилхлорид, при присоединении к последнему хлорноватистой кислоты образуются хлоргидрины, например, CH2ClCHOHCH2Cl, которые при омылении щёлочью превращаются в глицерин.
На превращениях аллилхлорида в глицерин через дихлоргидрин или аллиловый спирт основаны другие методы. Известен также метод получения глицерина окислением пропилена в акролеин; при пропускании смеси паров акролеина и изопропилового спирта через смешанный ZnO — MgO катализатор образуется аллиловый спирт. Он при 190—270 °C в водном растворе перекиси водорода превращается в глицерин.
глицерин можно получить также из продуктов гидролиза крахмала, древесной муки, гидрированием образовавшихся моносахаридов или гликолевым брожением сахаров. Также глицерин получается в качестве побочного продукта при производстве биотоплива.
Производные глицерина и их место в обмене веществ живых организмов
Глицериды
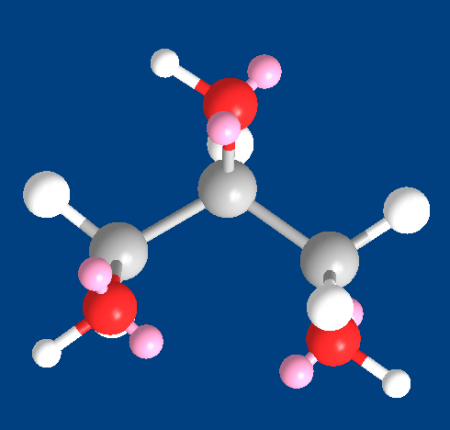
Триглицериды являются производными глицерина и образуются при присоединении к нему высших жирных кислот. Триглицериды являются важными компонентами в процессе обмена веществ в живых организмах.
Жиры и масла гидрофобны и нерастворимы в воде, так как гидроксильные группы глицерина заменены малополярными остатками жирных кислот.
Применение
Область применения глицерина разнообразна: пищевая промышленность, табачное производство, электронные сигареты, медицинская промышленность, производство моющих и косметических средств, сельское хозяйство, текстильная, бумажная и кожевенная отрасли промышленности, производство пластмасс, лакокрасочная промышленность, электротехника и радиотехника (в качестве флюса при пайке).
глицерин относится к группе стабилизаторов, обладающих свойствами сохранять и увеличивать степень вязкости и консистенции пищевых продуктов. Зарегистрирован как пищевая добавка E422, и используется в качестве эмульгатора, при помощи которого смешиваются различные несмешиваемые смеси.
Поскольку глицерин хорошо поддается желированию и горит без запаха и чада, его используют для изготовления высококачественных прозрачных свечей и основы для жидкости, используемой в дым-машинах.
Также глицерин используется при изготовлении динамита.
В последние годы глицерин используется, наряду с пропиленгликолем, в качестве основного компонента для приготовления жидкости и картриджей для электронных сигарет.
Используется в криобиологии и крионике как основной компонент популярных проникающих криопротекторов для криоконсервирования анатомических препаратов, биологических тканей и организмов.