Лантан
Лантан
| 57 |
Лантан
|
|
La
|
|
| 5d16s2 | |
Лантан — химический элемент 3-й группы (по устаревшей классификации — побочной подгруппы третьей группы) шестого периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 57, атомная масса — 138,9055. Обозначается символом La (лат. Lanthanum). Простое вещество лантан — блестящий металл серебристо-белого цвета, относится к редкоземельным элементам.
Содержание
История
Лантан как химический элемент не удавалось открыть на протяжении 36 лет. В 1803 г. 24-летний шведский химик Йёнс Якоб Берцелиус исследовал минерал, известный теперь под названием церит. В этом минерале была обнаружена иттриевая земля и ещё одна редкая земля, очень похожая на иттриевую. Её назвали цериевой. В 1826 г. Карл Мозандер исследовал цериевую землю и заключил, что она неоднородна, что в ней, помимо церия, содержится ещё один новый элемент. Доказать сложность цериевой земли Мозандеру удалось лишь в 1839 г. Он сумел выделить новый элемент, когда в его распоряжении оказалось большее количество церита.
Происхождение названия
Новый элемент, обнаруженный в церите и мозандерите, по предложению Берцелиуса назвали лантаном. Оно было дано в честь истории его открытия и происходит от др.-греч. λανθάνω — «скрываюсь», «таюсь».
Нахождение в природе
Лантан вместе с церием и неодимом относится к наиболее распространенным редкоземельным элементам. Содержание лантана в земной коре порядка 2,9·10−3% по массе, в морской воде — около 2,9·10−6мг/л. Основные промышленные минералы лантана — монацит, бастнезит, апатит и лопарит. В состав этих минералов также входят другие редкоземельные элементы.
Получение
Получение лантана связано с разделением исходного сырья на фракции. Лантан концентрируется вместе с церием, празеодимом и неодимом. Сначала из смеси отделяют церий, затем оставшиеся элементы разделяют экстракцией.
Физические свойства
Лантан — блестящий серебристо-белый металл, в чистом состоянии — ковкий и тягучий. Слабо парамагнитен. Кристаллическая структура плотноупакованная типа плотнейшей гексагональной упаковки.
Существует в трёх кристаллических модификациях: α-La с гексагональной решёткой (а=0,3772 нм, с=1,2144 нм, z=4, пространственная группа Р63/ттс), β-La с кубической решёткой типа меди (а=0,5296 нм, z=4, пространственная группа Fm3m), γ-La с кубической объёмноцентрированной решёткой типа α-Fe (а=0,426 нм, z=2, пространственная группа Im3m, устойчив до 920 °C) температуры переходов α↔β 277 °C и β↔γ 861 °C. DH° полиморфных переходов: α:β — 0,36 кДж/моль, β:γ — 3,12 кДж/моль. При переходе из одной модификации в другую меняется плотность лантана: α-La имеет плотность 6,162-6,18 г/см3, β-La — 6,19 г/см3, γ-La — 5,97 г/см3.
Сплавляется с цинком, магнием, кальцием, таллием, оловом, свинцом, никелем, кобальтом, марганцем, ртутью, серебром, алюминием, медью и кадмием. С железом лантан образует пирофорный сплав.
Химические свойства
По своим химическим свойствам лантан больше всего похож на 14 следующих за ним элементов, поэтому их называют лантаноидами. Металлический лантан обладает высокой химической активностью.
- Во влажном воздухе быстро превращается в основный карбонат лантана:
-
- 4La + 3O2 → 2La2O3
-
- La2O3 + 2CO2 + H2O → 2LaCO3(OH)
- При 450 °С сгорает в кислороде с образованием оксида лантана(III):
-
- 4La + 3O2 →450oC 2La2O3
- Медленно реагирует с холодной водой и быстро — с горячей, образуя гидроксид лантана (III):
-
- 2La + 6H2O →90oC 2La(OH)3 + 3H2↑
- При нагревании лантан вступает в реакции со фтором, хлором, бромом и йодом, давая соответственно фторид, хлорид, бромид и йодид:
-
- 2La + 3F2 →100oC 2LaF3
-
- 2La + 3Cl2 →100oC 2LaCl3
-
- 2La+ 3Br2 →toC 2LaBr3
-
- 2La + 3I2 →toC 2LaI3
- Легко взаимодействует с минеральными кислотами с образованием ионов La3+ и водорода. Вполне возможно, что в водном растворе ион La3+ в значительной степени существует как комплексный ион [La(OH2)9]3+:
-
- 2La + 3H2SO4 →H2O 2La3+ + 3SO42− + 3H2↑
Основные соединения
- Ацетилацетонат лантана — органическое соединение, хелат, формула La(C5H7O2)3. Представляет собой бесцветное твёрдое вещество, хорошо растворимое в воде и органических растворителях. Получается реакцией солей лантана со спиртовым раствором ацетилацетона.
- Бензоилацетонат лантана — хелатное соединение лантана, формула La(C10H9O2)3. Образует жёлтые призматические кристаллы. Получается взаимодействием солей лантана со спиртовым раствором бензоилацетона.
- Бромид лантана (III) — бинарное соединение, формула LaBr3. Образует белые кристаллы, хорошо растворимые в воде. Получают действием бромоводорода на оксид или сульфид лантана.
- Гидрид лантана (III) — бинарное соединение, формула LaH3. Представляет собой тёмно-синее кристаллическое вещество; реагирует с водой с образованием гидроксида лантана. Получается действием водорода на лантан при 210—290 °С.
- Гидроксид лантана (III) — белое нерастворимое в воде вещество с формулой La(OH)3. Образуется при действии горячей воды на металлический лантан или на оксид. При температурах выше 300 °С — разлагается.
- Йодид лантана (III) — бинарное соединение, формула LaI3. Образует кристаллы жёлто-зелёного цвета, хорошо растворимые в воде и органических растворителях. Получают нагреванием лантана и йода в инертной атмосфере.
- Карбид лантана (III) — бинарное соединение лантана с углеродом, формула LaС2. Образует жёлтые кристаллы. Реагирует с водой с образованием гидроксида и с выделением этана и ацетилена.
- Карбонат лантана (III) — бесцветное кристаллическое вещество с формулой La2(CO3)2, образует кристаллогидрат состава La2(CO3)2·8H2O. Получается пропусканием углекислого газа через суспензию гидроксида лантана.
- Купферонат лантана — органическое вещество, хелат, формула [La{C6H5N(NO)O}3]. Образует жёлтые кристаллы. Получается реакцией хлорида лантана с раствором купферона в кислой среде.
- Нитрат лантана (III) — бесцветное кристаллическое вещество с формулой La(NO3)3; хорошо растворяется в воде и органических растворителях. Получается растворением лантана, его оксида или гидроксида в азотной кислоте.
- Оксалат лантана (III) — бесцветное вещество, формула La2(C2O4)3. Не растворяется в воде. Получается действием на растворимые соли лантана избытком щавелевой кислоты.
- Оксид лантана (III) — белые кристаллы, формула La2O3. Не растворяется в воде, но медленно реагирует с ней. Получается сгоранием лантана на воздухе или разложением его солей при высоких температурах. Растворяется в кислотах с образованием солей La(III). На воздухе поглощает углекислый газ, постепенно превращаясь в основной карбонат лантана.
- Оксисульфид лантана — желтовато-белые гексагональные кристаллы с формулой La2O2S.
- Оксифторид лантана (III) — бесцветные кристаллы кубической сингонии, формула LaOF. Получают взаимодействием фторида лантана с водяными парами при 800 °С или спеканием оксида лантана с фторидом лантана в вакууме.
- Силицид лантана (III) — бинарное неорганическое соединение, формула LaSi2. Образует серые кристаллы.
- Сульфат лантана (III) — бесцветные кристаллы, растворимые в воде, формула La2(SO4)3. Получается растворением металлического лантана, его оксида или гидроксида в серной кислоте. Разлагается при нагревании.
- Сульфиды лантана — бинарные неорганические соединения лантана и серы. Сульфид лантана (III) имеет формулу La2S3; образует жёлто-красные кристаллы, нерастворимые в воде. Получается действием паров серы на лантан при 600—800 °С. Моносульфид лантана LaS — образует золотистые кристаллы кубической сингонии. Дисульфид лантана LaS2 — коричневые кристаллы.
- Фосфат лантана (III) — бесцветные кристаллы, плохо растворимые в воде, формула LaPO4. Получается обменной реакцией между растворимой солью лантана и фосфатом щелочного металла.
- Фосфид лантана (III) — бинарное неорганическое соединение, чёрные кристаллы с формулой LaP. Получается реакцией лантана и фосфора при 400—500 °С.
- Фторид лантана (III) — бесцветное вещество с формулой LaF3. Не растворяется в воде. Получают взаимодействием лантана с плавиковой кислотой либо прямым сгоранием лантана во фторе.
- Хлорид лантана (III) — бесцветное вещество с формулой LaCl3, хорошо растворимое в воде. Получается реакцией лантана с хлором или взаимодействием его с соляной кислотой.
Минералы
- Бастнезит — минерал класса фторкарбонатов, формула (Ce, La, Y)CO3F. Образует прозрачные кристаллы жёлтого, оранжевого, красного и бурого цветов. Твёрдость по Моосу — 4—4,5; удельный вес — 4,93—5,18. Может содержать от 34,7 до 45,8 % оксида лантана (III).
- Гадолинит — чёрный (чёрно-бурый) минерал с жирным стекловатым блеском, формула (Ce, La, Nd, Y)2FeBe2Si2O10. Твёрдость по шкале Мооса — 6,5-7. Удельный вес — 4-4,3. Состав непостоянен.
- Монацит — минерал класса фосфатов, формула (Ce, La, Nd, Th)[PO4]. Может иметь жёлтую, красновато-бурую, гиацинтово-красную, оливиново-зеленую окраску; цвет черты — белый (зеленовато-белый). Твёрдость по Моосу — 5—5,5; удельный вес — 4,9—5,2. Из-за высокого содержания урана и тория — радиоактивен.
- Ортит — бурый или чёрный минерал, класса силикатов. Химическая формула — (Ca, Ce, La, Y)2(Al, Fe)3(SiO4)3(OH). Твёрдость по Моосу — 5,5-6. Удельный вес составляет 3,3—3,8.
Применение
- Впервые в истории лантан применяли в газокалильных сетках. Австрийский химик Карл Ауэр фон Вельсбах использовал смесь, состоящую из 60 % оксида магния, 20 % оксида иттрия и 20 % оксида лантана, которая получила название Actinophor и была запатентована в 1885 году. Новый осветительный прибор («ауэровский колпачок») давал светло-зелёный свет.
- Оксид и борид лантана используются в электронно-вакуумных лампах как материал т. н. «горячего катода», то есть катода с высокой интенсивностью потока электронов. Кристаллы LaB6 применяются в источниках катодных лучей для электронных микроскопов.
- Лантан применяется как компонент сплавов никеля, магния, кобальта и др.
- Соединение состава La(Ni3.55Mn0.4Al0.3Co0.4Fe0.35) используется для анодного материала никель-металл-гидридных аккумуляторов. Оно представляет собой интерметаллид AB5-типа.
- Чистый лантан практически не используется по причине своей высокой стоимости; вместо него применяется мишметалл: сплав с содержанием лантана 20—45 %. Мишметалл является компонентом жаропрочных и коррозионностойких сплавов.
- Для производства типичного гибридного автомобиля Toyota Prius требуется 10—15 кг лантана, где он входит в состав аккумулятора.
- Карбонат лантана используется как лекарство, имеющее собственное название Fosrenol, применяющееся при гиперфосфатемии для поглощения избытка фосфатов.
- Лантан имеет свойство поглощать водород. Один объём этого вещества способен поглотить до 400 объёмов водорода в процессе обратимой адсорбции. Это свойство применяется для создания емких аккумуляторов водорода (металлогидридное хранение водорода) и в системах сохранения энергии, так как при растворении водорода в лантане выделяется теплота.
- Соли лантана и других редкоземельных элементов применяются в угольных дуговых лампах для увеличения яркости дуги. Угольные дуговые лампы были популярны в кинопроекторах. На производство последних приходится около 25 % соединений лантана, которые изначально предполагались для дуговых ламп.
- Жидким лантаном извлекают плутоний из расплавленного урана.
- Небольшая добавка лантана к стали увеличивает её пластичность и деформируемость. Добавка лантана к молибдену уменьшает его твёрдость и чувствительность к перепадам температур.
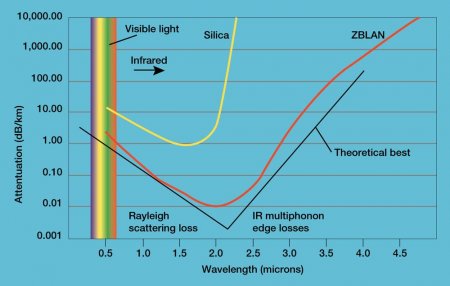
- Фторид лантана — важный компонент люминофоров. В смеси с фторидом европия он используется в кристаллической мембране ионоселективных электродов. Он также входит в состав стекла ZBLAN. Оно обладает улучшенным коэффициентом пропускания в инфракрасном диапазоне и поэтому применяется в волоконной оптике.
- Оксид лантана (III) — компонент специальных стёкол, высокотемпературной керамики, применяется также для производства других соединений лантана.
- Хлорид и бромид лантана применяются как сцинтилляторы с высоким световым выходом, лучшим энергетическим разрешением и временем высвечивания.
- Оксисульфид и алюминат лантана используются в люминофорах.
- Ионы лантана, как и пероксидаза хрена, используется в молекулярной биологии для усиления электрического сигнала до уровня, необходимого для детекции.
- Бентонитовая глина (т. н. Phoslock), в которой ионы натрия и кальция заменяются на ионы лантана, используется для очистки сточных вод от фосфатов.
- Небольшое количество соединений лантана связывает фосфаты в воде, в результате чего останавливается рост водорослей, которым необходимы соединения фосфора. Это свойство может применяться для очистки воды в бассейнах.
- Некоторые соединения лантана (и других редкоземельных элементов), например, хлориды и оксиды являются компонентами различных катализаторов, применяемых в частности, для крекинга нефти.
- Добавка оксида лантана (La2O3) к вольфраму используется при дуговой сварке вольфрамовым электродом, как замена радиоактивному торию.
- Лантан-бариевый метод радиометрического датирования иногда используется для оценки возраста горных пород и месторождений полезных ископаемых.
Биологическая роль
В 1930-х годах советский учёный А. А. Дробков исследовал влияние редкоземельных металлов на культурные растения. Он проводил опыты с горохом, репой и другими растениями, вводя в грунт редкоземельные элементы (РЗЭ) вместе с бором, марганцем или без них. Результаты опытов показывали, что редкоземельные элементы, в том числе лантан, улучшают рост растений. Однако использование микроудобрений на основе лантана и других РЗЭ приводит к противоположным результатам для разных видов и даже сортов одного вида культурных растений. В Китае, являющемся ведущим мировым производителем РЗЭ, такие микроудобрения массово применяются в сельском хозяйстве.
Ионы лантана способны увеличивать амплитуду ГАМК-активированных сигналов на пирамидальных нейронах гена CA1, отмеченных в гиппокампе головного мозга. Получение этих данных позволило сравнить чувствительность рецепторов ГАМКA пирамидальных нейронов с аналогичными рецепторами других клеток по восприимчивости к ГАМК и ионам лантана.
Изотопы
В природе лантан встречается в виде смеси двух изотопов: стабильного 139La и радиоактивного 138La (период полураспада 1,02⋅1011 лет). Доля более распространённого изотопа 139La в природной смеси составляет 99,911 %. Искусственно получены 39 неустойчивых изотопов с массовыми числами 117—155 и 12 ядерных изомеров лантана. Наиболее долгоживущим из них является лантан-137 с периодом полураспада около 60 тыс. лет. Остальные изотопы имеют периоды полураспада от нескольких миллисекунд до нескольких часов.
Меры предосторожности
Лантан относится к умеренно-токсичным веществам. Металлическая пыль лантана, а также мелкие частицы его соединений могут раздражать верхние дыхательные пути при попадании их внутрь, а также вызвать пневмокониоз.