Карбонат аммония
Карбонат аммония
| Карбонат аммония | |
|---|---|
 |
|
 |
|
| Традиционные названия | углекислый аммоний |
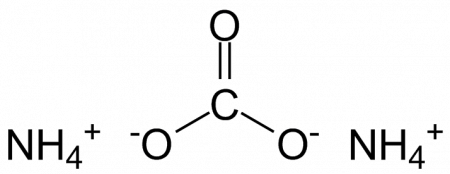
| Хим. формула | (NH4)2CO3 |
| Плотность | 1,6 г/см³ |
| Температура | |
| • разложения | 60 °C |
| Растворимость | |
| • в воде | растворим (0 °C) 100,1 (15 °C) Разл. (100 °C) |
| ГОСТ | ГОСТ 3770-75 ГОСТ 9325-79 |
| Рег. номер CAS | 506-87-6 |
| PubChem | 10480 |
| Рег. номер EINECS | 208-058-0 |
| SMILES |
C(=O)(O)O.N.N
|
| InChI |
1S/CH2O3.2H3N/c2-1(3)4;;/h(H2,2,3,4);2*1H3
PRKQVKDSMLBJBJ-UHFFFAOYSA-N
|
| Кодекс Алиментариус | E503i |
| ChEBI | 10048 |
| ChemSpider | 10048 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Карбонат аммония, углекислый аммоний, (NH4)2CO3 — аммониевая соль угольной кислоты.
Содержание
- 1 Свойства
- 2 Применение
Свойства
Бесцветные кристаллы соединения хорошо растворимы в воде. Карбонат аммония очень неустойчив как на воздухе, так и в растворе, так как уже при комнатной температуре выделяет аммиак, превращаясь в Гидрокарбонат аммония NH4HCO3. При температуре 60 °C быстро распадается на NH3, CO2 и H2O.
Подвергается гидролизу:
Применение
На процессе разложения, связанном с выделением газов, основано применение карбоната аммония вместо дрожжей в хлебопечении и кондитерской промышленности (пищевая добавка E503). Получают Карбонат аммония взаимодействием газообразных NH3, CO2 и H2O при быстром охлаждении продуктов реакции. Технический продукт содержит наряду с (NH4)2CO3 соединение гидрокарбоната аммония с карбаминатом аммония NH4HCO3 ⋅ NH4COONH2.
Карбонат аммония применяется для получения сульфата аммония из гипса по реакции
-
- (NH4)2CO3 + CaSO4 → (NH4)2SO4 + CaCO3
При этом Карбонат аммония можно вводить в виде раствора (жидкостный процесс конверсии), вместо карбоната аммония можно вводить газообразные NH3 и CO2 (газовый процесс конверсии), а также можно вводить газообразные NH3 и CO2 дополнительно к раствору (NH 4)2CO3 в количестве 10—15 % стехиометрического количества в расчёте на CaSO4 (газожидкостный процесс конверсии). В последнем случае при растворении газов выделяется дополнительная теплота, необходимая для протекания реакции. Карбонат аммония может рассматриваться как источник карбонат-ионов и в перспективе может применяться, например, для осаждения солей магния для отделения его от солей калия. При добыче калия из морской воды соли калия выделяются вместе с солями магния и не могут быть очищены от него перекристаллизацией. При добавлении карбоната аммония магний выпадает в осадок в виде карбоната, в растворе остаются в основном Хлорид калия и Хлорид аммония, которые впоследствии могут быть разделены (рекристаллизацией или возгонкой), либо не разделяться, а использоваться как азотно-калийное удобрение. Также Карбонат аммония применяется:
- в лекарственных препаратах (сиропы от кашля, нашатырь и др.);
- в качестве ускорителя ферментации при производстве вина;
- в качестве компонента огнетушащих составов
- в косметике в качестве красителей
- в качестве компонента раствора чистки стволов огнестрельного оружия (РЧС)


